Sistema immunitario - UniBa
←
→
Trascrizione del contenuto della pagina
Se il tuo browser non visualizza correttamente la pagina, ti preghiamo di leggere il contenuto della pagina quaggiù
sistema immunitario Sistema immunitario: sistema di cellule e molecole implicato nell’individuazione e contrasto di elementi estranei all’organismo (principalmente agenti infettivi, ma anche elementi di altra natura), capaci di comprometterne il benessere (omeostasi dell’organismo). Argomenti: ➢ Come i sistemi cellulari e molecolari descritti nell’infiammazione (immunità innata) attivano i sistemi cellulari e molecolari dell’immunità adattativa. ➢ Come agiscono i sistemi dell’immunità adattativa e come sono controllati ➢ Quali sono le cause e le conseguenze del malfunzionamento del sistema immunitario (immunopatologia).
Le malattie infettive
▪ Aspetti epidemiologici
• Importante causa di morbilità e mortalità (a livello globale, > 1/3 dei decessi nel 2009 sono
stati causati da malattie infettive).
• Negli USA, la polmonite è al 5° posto come causa di morte, ed è la più comune causa di
morte fra le malattie infettive.
• > 35 milioni di persone nel mondo sono attualmente affette dal virus HIV, e l’AIDS è
attualmente la principale causa di morte nell’Africa sub-Sahariana.
▪ Malattia infettiva (definizione)
• Condizione morbosa associata alla moltiplicazione di microbi (dai virus ai parassiti
multicellulari) nei tessuti dell’ospite.
• A volte, i microbi si moltiplicano sulla superficie o nel lume di organi cavi e producono
malattia producendo tossine che danneggiano le cellule (senza «invadere» i tessuti).
• A volte, i microbi possono causare malattia senza entrare di fatto in contatto con l’ospite,
ma attraverso le loro tossine (ad es. la tossina botulinica presente in alimenti non
correttamente manipolati).Il nostro organismo è in realtà un meta-organismo
il numero totale di cellule microbiche (microbiota) presenti sulla cute e in altre zone anatomiche è
≈ 10 volte più alto del numero totale delle cellule che compongono il nostro corpo.
Quali sono le funzioni del microbiota?
Ancora largamente inesplorate; fra quelle
finora individuate:
▪usare i nutrienti disponibili e occupare una
nicchia ecologica → competizione con
agenti patogeni.
▪produrre sostanze antibatteriche tossiche
per gli agenti patogeni.
▪indurre una risposta immunitaria crociata
nei confronti di agenti patogeni.
▪contribuire al corretto sviluppo della
risposta immunitariaLe malattie infettive sono causate da microbi «patogeni» e/o da microbi «opportunisti»
▪ Relativamente poche specie microbiche possono essere considerate «patogene».
▪ Fra le specie patogene, relativamente pochi cloni provocano malattia (ad es. streptococcus
pneumoniae penicillino-resistente, attualmente diffuso in tutto il mondo, deriva da pochi cloni
originatisi in Sudafrica e in Spagna).
▪ Le specie patogene hanno caratteristiche che favoriscono:
▪ la trasmissibilità
▪ la capacità di aderire alle superfici biologiche conferiscono la capacità di
▪ la capacità di invadere i tessuti determinare malattia
▪ la capacità di eludere le difese dell’ospite
fattori di virulenza
▪ Le specie opportuniste
▪ Non hanno particolari caratteristiche di virulenza, ma provocano malattia nell’ospite in cui i sistemi di
difesa sono compromessi
▪ Modalità di infezione
▪ Contatto diretto (ad es. stafilococco)
▪ Via aerea (microbi responsabili delle malattie infettive dell’app. respiratorio)
▪ Acqua contaminata (ad es. giardia, febbre tifoide)
▪ Alimenti (ad es. tossine di stafilococcus aureus)
▪ Sangue (ad es. virus epatitici, HIV)
▪ Via sessuale (treponema, neisseria, clamidia)
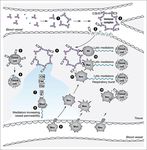
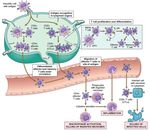
▪ Altre (trasmissione in utero, trasmissione via artropodi,...)Schema riassuntivo della risposta immunitaria: l’immunità innata
cellula tumorale;
cellula infettata da
microbi intracellulari
▪Le cellule NK riconoscono
direttamente ed eliminano
cellule anomale.
▪Si ritiene che sviluppino una
specifica modalità di
memoria, ponendosi al
confine fra immunità innata e
adattativa
natural killer
macrofago mastocita neutrofilo eosinofilo basofilo Cellula dendritica
▪Qualora l’ingaggio sia più severo,
▪Macrofagi e mastociti «residenti» sono le
▪I leucociti circolanti, principalmente assume maggiore rilievo il ruolo
prime cellule del sistema immunitario capaci
neutrofili, rispondono agli agenti patogeni in delle cellule dendritiche.
di rispondere all’ingaggio da parte di agenti
modo simile a quello di macrofagi e mastociti ▪Le DC, infatti, fagocitano gli agenti
patogeni.
e, in aggiunta, sostengono il reclutamento di patogeni e li degradano in modo
▪La risposta consiste nella fagocitosi, e nella
altri leucociti circolanti. da esporre sulla propria superficie
degranulazione di molecole con azione
strutture molecolari del patogeno
citotossica.
(antigeni).
▪Qualora l’ingaggio sia più severo, la risposta
▪Nella loro funzione di «cellule
di macrofagi e mastociti determina il
presentanti l’antigene» (APC), le
reclutamento di leucociti circolanti.
DC attiveranno le cellule
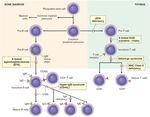
dell’immunità adattativa.Schema riassuntivo della risposta immunitaria: l’immunità adattativa
-cellula tumorale
-cellula infetta da
microbo intracellulare
-batterio
Le cellule TCD8+ diventano CTL (linfociti T
citotossici)
Le DC migrano nei linfonodi, Le cellule TCD4+ (Th) attivate diventano Th1, Th2, Th17 e
dove attivano le cellule TCD8+ producono vari segnali molecolari (ad es. interleuchine,
(Tc) e le cellule TCD4+ (Th) chemochine) che influenzano il comportamento delle
cellule TCD8+ e delle cellule B.
Le DC migrano nei Le cellule B attivate Gli anticorpi hanno varie funzioni
linfonodi, dove diventano plasmacellule effettrici nei confronti degli agenti
attivano le cellule B produttrici di anticorpi patogeni...com’è organizzato il sistema immunitario? Nella situazione operativa più comune (agenti infettivi), sono presenti tre livelli che operano in sequenza e in modo integrato ai fini della difesa e contrasto. 1. BARRIERE FISICHE: rivestimenti epiteliali superficiali; muco e altre secrezioni contenenti molecole anti-microbiche; barriere anatomiche interne (pleura, peritoneo, fasce etc). Modo d’azione: esclusione e/o confinamento. 2. IMMUNITÀ INNATA: i) cellule dell’immunità innata residenti nei tessuti e provenienti dal sangue; ii) mediatori solubili (ad es. complemento, proteine fase acuta). Modo d’azione: risposta pre-programmata e rapida, con ampia specificità conferita dal riconoscimento PAMP/DAMP-PRR, (infiammazione acuta). 3. IMMUNITÀ ADATTATIVA: cellule dell’immunità adattativa (linfociti B e T). Modo d’azione: le cellule B e T per mezzo di specifici recettori (BCR e TCR) riconoscono strutture molecolari (antigeni) dell’agente patogeno. La risposta viene memorizzata.
barriere fisiche (anatomo-funzionali)
fattori meccanici: barriera fisica delle superfici epiteliali; ruolo delle ciglia, della peristalsi,
lacrime, saliva, muco.
fattori chimici: varie sostanze con attività antimicrobica presenti in
▪ sudore: acidi grassi e pH acido
▪ saliva, lacrime e secrezioni nasali: lisozima e fosfolipasi
▪ succo gastrico: pH acido
▪ apparato respiratorio: defensine (1) e surfattante (2).
fattori biologici: la normale flora (cutanea, gastroenterica) previene la colonizzazione da
parte di patogeni.
(1) piccole proteine cationiche che interagiscono con la membrana cellulare microbica, alterandola.
(2) complesso fosfolipoproteico secreto dalle cellule alveolari (classe II) che riduce la tensione
superficiale alveolare.Cellule dell’immunità innata
cellule epiteliali, cellule -In risposta ad agenti infettivi e segnali di danno rilasciano vari segnali
endoteliali, mastociti molecolari (mediatori dell’infiammazione).
-Fagociti professionali sia residenti (MØ residenti) sia circolanti e rapidamente
neutrofili e
reclutabili dal sangue (neutrofili e monociti). Via interazioni PAMP/DAMP-PRR
monociti/macrofagi
riconoscono, fagocitano e distruggono agenti infettivi e altro materiale.
-Presenti nella maggior parte dei tessuti, hanno una ricca serie di PRR. Funzione
APC (antigen presenting cells): catturano materiale proteico, lo trasformano in
cellule dendritiche
oligopeptidi antigenici posizionati sulla propria superficie, e lo “presentano” alle
cellule T per il riconoscimento da parte dei TCR (T cell receptor).
cellule natural killer Riconoscono ed eliminano cellule infettate da virus e batteri intracellulari, e
(NK) cellule tumorali.
Cellule ILC (innate
Cellule simili a linfociti, ma con funzioni prevalenti di immunità innata.
lymphoid cells
Sistemi molecolari dell’immunità innata
complemento lisi delle cellule bersaglio, opsonizzazione, effetti pro-infiammatori.
Proteine della fase Proteine plasmatiche la cui concentrazione varia in presenza di
acuta infiammazione, con varie azioni (vedi).Recettori dell’immunità innata
PRR. Fagociti, cellule dendritiche (e anche molti
tipi di cellule epiteliali) esprimono varie classi di
PRR capaci di rilevare la presenza di agenti
microbici (PAMP) e prodotti del danno cellulare
(DAMP).
Le quattro principali classi di PRR comprendono:
▪ TLR (Toll-like receptors), membrana plasmatica
ed endosomi, recettori di vari prodotti
microbici
▪ NLR (NOD-like receptors), recettori citosolici
per peptidoglicani e vari DAMP
▪ CLR (C-type lectin receptors), recettori di
membrana per polisaccaridi microbici
▪ RLR (RIG-like receptors), recettori citosolici per
acidi nucleici.
Nell’insieme, sono stati identificati circa 100 diversi PRR capaci di riconoscere circa 1000 PAMP/DAMP.
Nell’immunità adattativa, come si vedrà, ci sono solo due tipi di recettori (BCR e TCR), ma sono
presenti in milioni di varianti capaci di riconoscere altrettanti antigeni.Interazioni PAMP-PRR
(pathogen-associated molecular patterns – pattern recognition receptors)
PAMP PRR localizzazione funzione
Recettori toll-like
Acidi lipoteicoici TLR2 Monociti, macrofagi, Attivazione dei fagociti,
LPS batterico TLR4 neutrofili, DC immature, produzione di citochine pro-
Flagellina batterica TLR5 cellule NK, alcune cellule T e infiammatorie, preparazione
Lipopeptidi di micoplasma TLR6 B, alcune cellule non immuni delle DC
ssRNA virale TLR7,8
dsRNA virale TLR3
DNA batterico (CpG non TLR9
metilate)
Monociti, macrofagi, DC,
Componenti parete batterica Recettori scavenger endotelio epatico Attivazione dei fagociti
Antigeni di cellule infette, Cellule NK Lisi cellula bersaglio,
stressate o tumorali Recettore NK produzione di citochine pro-
infiammatorie
Antigeni di cellule infette, cellule Tγδ Lisi cellula bersaglio,
stressate o danneggiate TCRγδ produzione di citochine pro-
infiammatorie
Antigeni glicolipidici Recettore NKT Cellule NKT produzione di citochine
PRM (solubili)
Polisaccaridi microbici Collectine (MBL), Proteine di plasma Attivazione del
fase acuta complemento, Fagocitosi
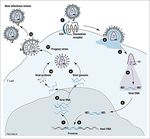
Peptidoglicani batterici Proteine NOD Citoplasma cellulare Produzione di citochine...cosa accade in una cellula dell’immunità innata quando un PRR è
ingaggiato dal corrispondente PAMP/DAMP?
Si producono distinte risposte preprogrammate, che dipendono dalla tipologia dell’interazione PAMP-
DAMP/PRR e dal tipo di cellula.
TLR. Nel caso dell’attivazione
TLR, vengono avviati segnali
molecolari che portano
all’attivazione del programma
trascrizionale NFkB (produzione
di citochine e di molecole di
adesione ai fini del
reclutamento e dell’attivazione
di leucociti), e IRF (produzione
di citochine antivirali come IFN
di tipo I).Recettori NLR e inflammasoma
Inflammasoma. Complesso proteico
che si forma nel citosol a seguito della
presenza di materiale da cellule morte
e di alcuni microbi. É costituito da una
proteina NLR, una proteina adattatrice
e dalla pro-caspasi 1, che viene attivata.
La caspasi 1 taglia la pro-IL1β (trascritta
a seguito dell’attivazione NFkB),
producendo la forma attiva IL1β.
Rilevanza patologica.
▪ Sindromi autoinfiammatorie
(condizione febbrile periodica
associata a mutazioni dominanti in
NLR).
▪ Urati (gotta), lipidi (obesità e diabete)
e cristalli di colesterolo (aterosclerosi)
possono attivare NLR, così
contribuendo all’infiammazione
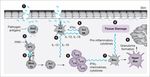
associata a tali condizioni.Infiammazione: Citochine, frammenti del complemento (e altri mediatori) prodotti
durante le reazioni dell’immunità innata attivano le modificazioni
vascolari e cellulari dell’infiammazione. I leucociti reclutati
eliminano i microbi e le cellule danneggiate.
Difesa antivirale: IFN di tipo I prodotti in risposta all’infezione virale agiscono su
cellule infette e non, determinando l’attivazione di enzimi che
degradano gli AN virali e inibiscono la replicazione virale: “stato
antivirale”.
Avvio e regolazione Produzione di segnali molecolari che avviano e stimolano la
della risposta risposta immunitaria adattativa.
adattativadenominazione protagonisti azione
Contrasto di microbi
Umorale anticorpi (o immunoglobuline), e
extracellulari e delle loro
(o anticorpale) linfociti B (o cellule B)
tossine.
Cellulare Contrasto di microbi
Linfociti T (o cellule T)
(o cellulo-mediata) intracellulari.
Il riconoscimento dell’agente patogeno è effettuato da recettori delle cellule B (BCR) e T (TCR),
capaci di riconoscere una varietà pressoché illimitata di strutture molecolari chiamate antigeni.
Antigene: entità molecolare che si può legare a BCR o TCR.
É costituito generalmente da pochi residui peptidici o glicidici (epitopo) che fanno parte di
strutture molecolari più grandi appartenenti a un agente infettivo, a cellule tumorali, a materiale
inerte dannoso, o a un tessuto proprio (self).Linfociti B Linfociti T
Riconoscono antigeni di varia natura (proteica, Riconoscono antigeni peptidici associati a molecole
glicidica, lipidica...) sia in fase fluida sia sulla MHC (pMHC) sulla superficie cellulare.
superficie cellulare.
▪ In particolare, in base alla tipologia di riconoscimento,
▪ Nelle condizioni appropriate, si attivano e si distinguono:
proliferano (espansione clonale). ▪ linfociti Th (o CD4+) (T helper)
▪ linfociti Tc (o CD8+)(T citotossici)
▪ Si differenziano in cellule effettrici, ▪ Nelle condizioni appropriate, si attivano, proliferano
plasmacellule, che producono anticorpi. (espansione clonale) e si differenziano in cellule
effettrici:
▪ Gli anticorpi:
▪ Th1 Produzione di citochine per la
▪ neutralizzano agenti microbici e tossine
Th ▪ Th2 regolazione della funzione di altre
▪ facilitano la fagocitosi cellule dell’immunità (T, B, MØ).
▪ Th17
▪ attivano il sistema complemento
CTL (linfociti T citotossici): eliminano cellule infette da
Tc
microbi intracellulari.
▪ Quando una cellula B o T viene attivata per la prima volta (risposta primaria), sarà prodotto un
clone di cellule effettrici che verranno eliminate al termine della risposta, e cellule B o T della
memoria a lunga vita.
▪ Quando una cellula B o T della memoria sarà attivata a seguito di un successivo incontro con
l’antigene (risposta secondaria), verrà di nuovo prodotto un clone di cellule effettrici e cellule B
o T della memoria.Come si genera una varietà pressoché illimitata di recettori BCR e TCR?
Il processo ha luogo durante la maturazione delle cellule B e T: Ricombinazione somatica. I geni che codificano
per BCR e TCR (≈400) sono presenti in tutte le cellule dell’organismo, ma solo i linfociti T e B contengono geni
ricombinati che derivano dall’azione di enzimi RAG-1 e RAG-2 -recombination activating genes).
Ricombinazione V-D-J (finalizzata alla sintesi di una
porzione del recettore BCR (catena pesante). Si noti
come il prodotto finale Vh-Dk-Jp-Cμ deriva da una
selezione casuale operata su molteplici segmenti che
vengono riarrangiati.
La combinazione fra molteplicità dei segmenti a
disposizione e scelta casuale è sufficiente a generare la
diversità recettoriale (107-109).
Ogni singola cella B o T prodotta (e le cellule figlie, cioè
nell’insieme il «clone» linfocitario), è caratterizzata da
una singola e specifica tipologia di recettore (BCR o
mRNA Vh-Dk-Jp-Cμ BCR (catena pesante) TCR), capace di riconoscere uno specifico antigene, e
presente in numerose copie sulla superficie cellulare.TCR è formato da un eterodimero αβ (o γδ) e possiede una regione variabile (VDJ) ed una regione costante (C). La regione variabile con le porzioni CDR1 e CDR2 riconosce MHC, mentre con la porzione CDR3 riconosce l’antigene (p). Il complesso del TCR è formato dalle molecole CD3 e dalla coppia ζζ. Il BCR (o immunoglobulina di membrana) è formato da due catene pesanti e due catene leggere. Ci sono 5 tipi possibili di catene pesanti (α,γ,δ, μ,ε), e due tipi di catene leggere (κ e λ). Anche nel caso di BCR c’è il complesso del BCR, costituito da Igα e Igβ. La regione Fab (sulle catene pesanti e su quelle leggere) riconosce l’antigene.
TCR, complesso del TCR, e co-recettori CD4 e CD8. TCR. Il 90% delle cellule T ha recettori TCRαβ. Le catene α e β hanno domini costanti C e variabili V (in questi ultimi sono presenti le regioni ipervariabili derivanti dalla ricombinazione genica). Complesso del TCR. É costituito da CD3 (catene γ, δ ed ε) e dalle catene ζ. Il complesso trasmette all’interno della cellula il segnale generato dal riconoscimento fra TCR e peptide antigenico associato a MHC. Co-recettori CD4 e CD8. Ai fini dell’attivazione della cellula T, il segnale trasmesso dal complesso del TCR deve essere amplificato dall’interazione dei co-recettori CD4 o CD8, rispettivamente con le molecole MHC di classe II o di classe I alle quali è associato il peptide antigenico. Il 60% delle cellule T esprime il recettore TCRαβ Il 30% delle cellule T esprime il recettore TCRαβ assieme al co-recettore CD4, e riconosce peptidi assieme al co-recettore CD8, e riconosce peptidi antigenici associati a MHC di classe II: cellule Th o antigenici associati a MHC di classe I: cellule Tc o TCD4+. TCD8+.
I segnali co-stimolatori e l’attivazione delle cellule Th *
▪ TCR, complesso del TCR e co-recettori CD4
determinano nell’insieme il riconoscimento
dell’antigene (segnale 1).
▪ Tuttavia, ai fini dell’attivazione ottimale delle cellule T,
è necessario il contributo di segnali co-stimolatori,
rappresentati dall’interazione fra recettore co-
stimolatore CD28 (sulla cellula T) e recettore
CD80/CD86 sulla cellula che presenta l’antigene pMHC
(APC) (segnale 2).
▪ Il segnale di co-stimolazione CD28-CD80/CD86
induce nella cellula T la sintesi di fattori di crescita e
proliferazione, e di Bcl2 anti-apoptotiche.
▪ Se al posto di CD28 la cellula T esprime CTLA-4 o PD-1,
queste competeranno per CD80/CD86 e l’effetto sarà
l’inibizione dell’attivazione della cellula T.
▪ NB: vi sono anche altre interazioni di co-stimolazione
(ad es fra CD2 della cellula T e LFA3 di APC):
nell’insieme, è la «sinapsi immunologica».
*L’attivazione delle cellule Tc avviene in modo simile, con la differenza che il segnale 1 è costituito
dal TCR che riconosce pMHC classe I, e dal co-recettore CD8 che riconosce MHC classe I.linfociti T: generalità, principali tipi e funzioni
▪ Le cellule T si sviluppano nel timo, da precursori di derivazione midollare.
▪ Rappresentano il 60-70% dei linfociti circolanti.
▪ Riconoscono antigeni presentati da altre cellule mediante il recettore TCR (eterodimero αβ, con
porzione costante e porzione variabile).
▪ Il TCRαβ riconosce esclusivamente peptidi antigenici associati a molecole MHC (major
histocompatibility complex) sulla superficie di altre cellule (restrizione MHC).
Linfociti T helper (Th, ▪ Sono attivati da cellule APC che presentano pMHC di classe II
o TCD4+) ▪ Stimolano i linfociti B a produrre anticorpi
▪ Attivano la funzione microbicida dei fagociti professionali
Linfociti T citotossici (Tc, o ▪ Sono attivati da cellule APC che presentano pMHC di classe I
TCD8+) ▪ Uccidono le cellule infettate da microbi intracellulari
Linfociti T regolatori (Treg) Limitano la risposta immunitaria, e prevengono la risposta
immunitaria verso antigeni propri.Cellule T, in base alle strutture molecolari impegnate nel riconoscimento antigenico
co- antigene quantità
TCR funzione
recettore riconosciuto relativa
Th (citochine per la
peptide associato a
cellule Th (TCD4+) TCRαβ CD4 60% funzione delle cellule B
MHC classe II
e dei MØ)
Tc (CTL) (uccidono
peptide associato a
cellule Tc (TCD8+) TCRαβ CD8 30% cellule infette da
MHC classe I
microbi intracellulari)
lipidi e
glicolipidi
associati a Immunità
cellule Tγδ TCRγδ - -
MHC-like, o mucosale
anche non
processati
TCRαβ glicolipidi Immunità
cellule NK-T - -
(invarianti) associati a CD1 mucosalelinfociti B. Si sviluppano da precursori midollari, e sono il 10-20% dei linfociti circolanti.
• I recettori BCR sono IgM associate
alla membrana
• I recettori BCR riconoscono
antigeni peptidici, lipidici e
polisaccaridici sia solubili sia
associati alla superficie cellulare.
• Dopo l’attivazione, i linfociti B
daranno luogo alla formazione di
plasmacellule produttrici di
anticorpi.
Struttura dei BCR
• Il BCR è costituito da una immunoglobulina (Ig) di membrana di tipo IgM (o IgD) che riconosce
l’antigene, e da un dimero associato (Igα-Igβ), con funzioni simili a quelle di CD3 delle cellule T.
• CD21 (o CR2) è il co-recettore per frammenti del complemento derivati da C3, e promuove
l’attivazione delle cellule B (segnale 2).Nel sistema immunitario più tipi cellulari denominati APC (cellule
presentanti l’antigene) sono capaci di catturare antigeni e presentarli
ai linfociti. Le cellule più importanti implicate nella presentazione di
antigeni peptidici alle cellule T sono le cellule dendritiche (DC).
▪ Le DC originano nel MO, e i precursori immaturi raggiungono tutti i
tessuti, dove risiedono come DC immature (iDC). Hanno molti
prolungamenti citoplasmatici, dotati di un’ampia varietà di PRR, che si
estendono a coprire un’ampia area.
▪ Le iDC campionano continuamente l’ambiente in cui risiedono (endocitosi e fagocitosi mediate dalle
interazioni PAMP-DAMP/PRR). In presenza di un agente infettivo, le iDC internalizzano il microbo e lo avviano
alla degradazione fagolisosomiale.
▪ Contemporaneamente, le iDC si muovono entrando nei vasi linfatici e migrano verso i linfonodi tributari
(seguendo il gradiente di chemochine come CCL19 e CCL21). Durante il viaggio, le iDC, dette DC convenzionali
migratorie, vanno incontro a maturazione:
▪ Elaborano pMHC (p = peptidi provenienti dalle proteine microbiche degradate) e li posizionano sulla
superficie cellulare.
▪ Elaborano e posizionano sulla superficie cellulare i segnali necessari per la co-stimolazione (ad es.
CD80/CD86).
▪ Le mDC raggiungono i linfonodi e, nella zona paracorticale, «presentano» pMHC alle cellule T.
▪ Altre popolazioni di DC (in aggiunta alle DC convenzionali migratorie)
▪ DC follicolari risiedono nei follicoli linfoidi, e catturano antigeni legati ad anticorpi o al complemento (hanno
recettori FcR per IgG e recettori per il frammento C3b). Presentano l’antigene alle cellule B, e selezionano le cellule
B con la più alta affinità fra BCR e antigene.
▪ DC plasmacitoidi, presenti in circolo e negli organi linfoidi sono la fonte principale di IFN di tipo I (risposta
antivirale).Macrofagi nella risposta adattativa
Anche i macrofagi sondano il
microambiente del tessuto in cui si
trovano, avendo anch’essi un’ampia
varietà di recettori PRR.
▪ Come le DC, anche i MØ
fagocitano microbi, e producono
pMHC classe II (p = peptide di
provenienza microbica),
associandoli alla propria
superficie.
▪ I pMHC classe II saranno
presentati a cellule Th (effettrici o
della memoria).
▪ si iperattivano in risposta a
citochine di T attivati, e con le
citochine prodotte amplificano le
risposte di cellule T e B
(reciprocità)Sistema MHC (sistema maggiore di istocompatibilità), noto anche come HLA (nell’uomo)
(sistema molecolare per la presentazione di antigeni peptidici alle cellule T)
- complessi proteici altamente polimorfici
- codificati da ≈200 geni sul cromosoma 6, raggruppati in tre classi:
- MHC classe I (HLA-A, HLA-B, HLA-C)
- MHC classe II (HLA-DP, HLA-DQ, HLA-DR)
- MHC classe III (componenti solubili: fattori del complemento, citochine)
L’elevato polimorfismo (migliaia di varianti), fa sì che le molecole MHC (classe I e II) di
ciascun individuo abbiano un certo grado di diversità rispetto alle molecole MHC di
ogni altro individuo (da grandi diversità fra soggetti non consanguinei, a diversità più
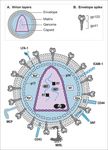
moderate fra consanguinei, fin quasi alla mancanza di diversità nei gemelli identici).MHC classe I. Proteine espresse su tutte le cellule
nucleate (e sulle piastrine).
▪ eterodimeri formati da una catena α (codificata da
HLA-A, HLA-B, e HLA-C) e da β2-microglobulina. Il
peptide antigenico (in rosso) è associato alla
porzione extracellulare della catena α; il
polimorfismo in questa regione è alla base della
capacità di MHC classe I di legare peptidi diversi.
Funzione: presentazione di peptidi provenienti da proteine intracitoplasmatiche (normali e non). Le
proteine del citosol sono degradate nel sistema proteasomico → i peptidi risultanti sono trasportati nel
RE ed associati a MHC classe I e quindi a β2-microglobulina → il complesso p-MHC classe I è trasportato
sulla superficie cellulare → pMHC classe I è “ispezionabile” dalle cellule TCD8+.
Implicazioni:
▪ tutte le cellule nucleate possono essere infettate da virus, e quando le cellule infette presentano
sulla propria superficie p-MHC classe I (p = polipeptide derivante da una proteina virale), vengono
riconosciute dalle cellule TCD8+ ed eliminate.
▪ tutte le cellule nucleate possono diventare tumorali. Le cellule TCD8+ possono riconoscere le cellule
tumorali per la presenza di p-MHC classe I (dove p = polipeptide derivante da una proteina espressa
solo o prevalentemente dalla cellula tumorale).MHC classe II. Espresse sulle APC (cellule presentanti
l’antigene) (DC, macrofagi, linfociti B). Eterodimeri α e β
codificati da HLA-DP, HLA-DQ, e HLA-DR. Il peptide
antigenico (in rosso) è associato sia ad α che a β. Il
polimorfismo in questa regione è alla base della capacità
di associare peptidi diversi.
Funzione: presentazione di antigeni che derivano da materiale proteico
internalizzato dalla cellula. Il materiale presente in fagosomi ed endosomi è digerito a
seguito della fusione lisosomiale; nelle vescicole stesse i peptidi risultanti sono
associati a MHC classe II e quindi trasportati sulla superficie, per essere presentati a
cellule TCD4+.
Implicazioni: quando una DC (o un macrofago) internalizza un microbo, la presenza di
p-MHC classe II sulla sua superficie è in grado di attivare una cellula TCD4+ che, con la
sua azione successiva, ottimizzerà l’eradicazione degli agenti infettivi.Processazione dell’antigene, formazione dei complessi pMHC, e presentazione dell’antigene. pMCH classe I. Le proteine del citosol sono degradate nel proteasoma e trasportate da TAP nel RE. Dopo la loro formazione, pMHC classe I pervengono sulla superficie cellulare (tutte le cellule nucleate). pMHC classe II. Il materiale proteico di provenienza extracellulare viene internalizzato in endosomi o in fagosomi dalle APC (DC, MØ, B). Con la riduzione del pH, le proteasi di derivazione lisosomiale digeriscono le proteine in corti polipeptidi. Dopo la fusione con vescicole contenenti MHC II, si formano pMHC II, e i complessi sono trasportati sulla superficie cellulare.
Linfociti NK. 5-10% dei linfociti circolanti, uccidono cellule anomale (ad es. tumorali) e/o
infette (ad es. da virus). Sono capaci di riconoscere le cellule da eliminare, ma non lo fanno
tramite recettori BCR o TCR.
Linfociti NK: caratteristiche e funzioni
Regolazione Dipende dall’equilibrio fra recettori
dell’attività di attivazione (ad es. NKG2D) e
citotossica recettori di inibizione (recettori per
MHC di classe I). La cellula normale,
esprimendo MHC classe I sulla
propria superficie, ingaggia i
recettori di inibizione, e non viene
uccisa. Al contrario, una cellula
infettata da virus (e anche le cellule
tumorali) aumenta l’espressione di
ligandi per i recettori di attivazione
delle NK, e riduce l’espressione di
MHC classe I sulla superficie,
venendo così uccisa.
citochine Producono IFN-γ (attivazione dei
MØ), e proliferano in risposta a varie
citochine
Recettori Citotossicità cellulo-mediata
per Fc di anticorpo-dipendente.
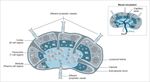
IgGOrgani, cellule, e organizzazione generale del sistema immunitario adattativo
2 x1012 linfociti (1), distribuiti in organi linfoidi primari e secondari, capaci di riconoscere
107-109 strutture antigeniche diverse.
organi linfoidi primari
midollo, e timo, dove i progenitori linfoidi
proliferano e si differenziano in linfociti B (midollo)
e linfociti T (timo) maturi (naive, o vergini), dotati
di recettori di membrana (BCR, TCR) per specifici
antigeni. Attraverso la circolazione, i linfociti B e T
maturi raggiungono gli
organi linfoidi secondari
linfonodi, milza, e tessuti linfoidi associati a varie
sedi anatomiche. Qui, i linfociti maturi possono
NALT (nasal-associated lymphoid tissue). SALT (Skin-associated incontrare l’antigene specifico che sono abilitati a
lymphoid tissue). GALT (gut-associated lymphoid tissue). BALT
(bronchial-associated lymphoid tissue riconoscere, e attivarsi.
(1) massa paragonabile a quella del fegato o del cervello, necessaria per l’ampiezza delle superfici da
presidiare (cute, 2 mq; mucose respiratorie e intestinali, 100 e 400 mq).il viaggio dei linfociti fra sangue e tessuti linfoidi: la ricircolazione linfocitaria Il numero dei linfociti naive per un dato antigene è molto basso (1/105-106); per aumentare la probabilità di incontro, i linfociti continuamente ricircolano fra sangue e organi linfoidi (dove avviene il contatto con l’antigene).
distribuzione dei linfociti B e T nei linfonodi Incontro con l’antigene e attivazione A seguito dell’incontro con l’antigene, le cellule B o T mature si attivano, proliferano, e si differenziano in cellule effettrici (a vita breve) e cellule della memoria (a vita lunga).
citochine nella risposta immunitaria
cellule produttrici effetti funzionali
citochine
(principali) (principali)
TNF, IL-1, IL-12, MØ, DC, NK, cellule
Immunità Indurre l’infiammazione e inibire la
innata
IFN tipo I, IFN-γ, e endoteliali e cellule
replicazione virale
chemochine epiteliali
Promuovere proliferazione e
IL-2, IL-4, IL-5,
TCD4+ attivati differenziazione dei linfociti, e
Immunità IL-17, e IFN-γ
adattativa attivare cellule effettrici.
Limitare e terminare la risposta
IL-10, TGF-β MØ, Treg
immunitaria.
Implicazioni: la conoscenza dei segnali molecolari coinvolti nella determinazione della
risposta immunitaria ha importanti implicazioni terapeutiche: molti farmaci che
antagonizzano l’attività di citochine sono attualmente progettati (alcuni usati) per il
controllo di patologie su base immuno-infiammatoria.Schema generale delle fasi della risposta immunitaria adattativa
Presentazione ▪ le APC (DC) presentano pMHC alle cellule T, selezionando e attivando il clone
dell’antigene cellulare che tramite TCR riconosce specificamente l’antigene presentato.
▪ le cellule B riconoscono antigeni di varia natura chimica, sia liberi sia associati a
cellule.
Attivazione linfocitaria ▪ Durante la risposta innata, le DC a seguito dell’interazione PAMP-PRR presentano
sulla propria superficie molecole di costimolazione (ad es CD80/CD86), che saranno
riconosciuti da recettori di superficie delle cellule T (ad es CD28) naive. Per
l’attivazione di una cellula T sono quindi necessarie le interazioni: pMHC-TCR (segnale
1), e segnali di costimolazione (segnale 2). Si noti che la DC presenta il segnale 2 solo
se è stata attivata da PAMP/PRR (cioè ha riconosciuto un’infezione microbica). Nella
risposta nei confronti di cellule tumorali, il segnale 2 può derivare dall’interazione
DAMP/PRR.
▪ Attivazione dei linfociti B, e produzione di anticorpi (non riassunta in questa
diapositiva).
Eliminazione ▪ attivazione dei linfociti T, espansione clonale, ed eliminazione dell’antigene (microbi
dell’antigene intracellulari; immunità cellulo-mediata o cellulare).
▪ Attivazione dei linfociti B, espansione clonale, ed eliminazione dell’antigene (microbi
extracellulari; immunità umorale).
Declino della risposta ▪ le cellule effettrici prodotte durante la risposta muoiono dopo l’eliminazione del
immune, e memoria microbo (apoptosi).
immunitaria. ▪ Memoria immunologica: l’iniziale attivazione linfocitaria genera anche cellule a
lunga sopravvivenza: in pratica, aumenta il numero dei linfociti capaci di riconoscere
l’antigene incontrato; inoltre, nell’eventualità di un incontro successivo con
l’antigene, le cellule della memoria rispondono con maggior rapidità ed efficacia
rispetto alle cellule naive.Attivazione e funzione delle cellule TCD4+: aspetti di maggiore rilievo
Espansione clonale, con Nel processo di attivazione le TCD4+ secernono IL2 e al contempo espongono
produzione di cellule sulla propria superficie IL2R: l’effetto è quello della proliferazione con aumento
effettrici e cellule della del numero di cellule TCD4+ capaci di riconoscere l’antigene attivante.
memoria.
cellule effettrici ▪ svolgono funzioni nell’organo linfoide (vedi)
▪ entrano in circolo, raggiungono la sede del processo che ne ha originato
l’attivazione, e operano ai fini della distruzione dell’antigene.
Interazione del ▪ TCD4+ naive↔DC: effetto di costimolazione per la TCD4+, e di completamento
recettore CD40L (cellula della maturazione della DC (DC autorizzata).
TCD4+) con il recettore ▪ TCD4+ effettrice↔cellula B: completamento dell’attivazione della cellula B
CD40 (cellula partner)* (switch isotipico e maturazione dell’affinità).
▪ TCD4+ effettrice↔macrofago: in aggiunta all’azione di IFNγ, determina
attivazione (classica) dei macrofagi.
sottotipi di cellule ▪ Th1
effettrici ▪ Th2
▪ Th17
* si ricordi che questa interazione si aggiunge a quella fra TCR e pMHC classe II e a quella fra CD4 e MHC classe IIIn relazione:
▪ alla modalità con cui la DC è stata
attivata ed è maturata
▪ alle citochine prodotte dalla DC al
momento dell’attivazione della
cellula T
possono svilupparsi tre tipi di Th,
funzionalmente distinti:
Th1, Th2, Th17.
citochine inducenti IFNγ, IL12 IL4 TGFβ, IL1, IL6, IL23
citochine prodotte IFNγ IL4, IL5, IL13 IL17, IL22, chemochine
attivazione di macrofagi, e attivazione di mastociti e di
risposte effettrici produzione di IgG eosinofili, produzione di IgE
reclutamento PMN
contrasto di microbi contrasto di microbi
ruolo benefico intracellulari contrasto di elminti
extracellulari, e funghi
ruolo patologico
(in caso di reazione infiammazione cronica infiammazione cronica
immuno-mediata (spesso allergie immuno-mediata (spesso
eccessiva / non autoimmunità) autoimmunità)
controllata)Dopo l’attivazione da parte di una DC autorizzata, una
cellula TC naive prolifera e si differenzia in cellule pre-
CTL, che lasciano il linfonodo per dirigersi al sito di
attacco dell’agente patogeno.
In tale sede, IL12, IL6 e IFNγ (da macrofagi e DC)
inducono la differenziazione dei pre-CTL in CTL
«armati». Questo processo si compie in 24-48 h
dall’attivazione della TC naive.
I CTL «armati» che incontrano l’appropriato pMHC classe
I sulle cellule dell’ospite le identificano come bersaglio e
ne determinano la morte (apoptosi)
▪ rilasciando il contenuto di granuli (perforina e serin-
proteasi)
▪ ingaggiando il recettore Fas
▪ rilasciando TNFDopo attivazione, le cellule B naive diventano plasmacellule (PC), che possono produrre vari tipi di anticorpi (Ab) con distinte funzioni. Immunità umorale. Un linfocita B naive riconosce l’antigene e –sotto l’influenza di Th (o di altri stimoli)- prolifera e si differenzia in PC anticorpo-secernenti. In alcuni casi, le PC producono Ab IgM, con catena pesante uguale a quella del BCR (IgM). In altri casi, durante il processo di differenziazione, la cellula B attivata modifica la catena pesante del recettore BCR, che diventa IgG (switch isotipico) e così diventerà una PC che produce IgG. Durante il processo di maturazione, la B attivata può migliorare l’affinità del proprio recettore per l’antigene, producendo IgG con più alta affinità per l’antigene (da queste cellule deriveranno le cellule della memoria). Il cambiamento isotipico può dare luogo a IgA (Ab secretori, immunità mucosale) e a IgE (Ab per l’attivazione di mastociti ed eosinofili (non mostrato).
Una cellula B naive può riconoscere antigeni peptidici, lipidici e polisaccaridici sia solubili sia
associati alla superficie cellulare: che tipo di PC diventerà dopo l’attivazione dipende
largamente dal tipo di antigene responsabile.
tipo di antigene meccanismo di attivazione effetto
Antigeni polisaccaridici e lipidici Per la loro struttura, epitopi ripetuti La cellula B produrrà PC a vita
(spesso costituiti da più epitopi ingaggiano più BCR sulla cellula B, breve, produttrici di IgM.
identici ripetuti, non possono attivandola (attivazione T-
essere riconosciuti da cellule T). indipendente)
Antigeni proteici ▪ La cellula B riconosce un epitopo ▪ Nel coniugato B-T, per effetto
peptidico tramite BCR dell’interazione CD40-CD40L e
▪ internalizza l’intera proteina dell’azione di citochine (IFNγ e
(endosoma) e la processa per IL4), avranno luogo i processi di
produrre pMHC classe II sulla switch isotipico e di maturazione
propria superficie. dell’affinità, allo scopo di variare
▪ una cellula Th effettrice riconosce e migliorare la qualità della
pMHC classe II, e si formerà così risposta anticorpale.
un coniugato B-T (attivazione T- ▪ Le PC che deriveranno saranno a
dipendente). vita lunga, migreranno nel MO e
per molto tempo produrranno
Ab.
▪ Si produrranno anche cellule della
memoria.come la cellula B risponde
ad antigeni Td
altre cellule B modificano la struttura del BCR, aumentandone
alcune cellule B si differenziano l’affinità per l’antigene (ipermutazione somatica e maturazione
in PLASMACELLULE A VITA BREVE dell’affinità). Sopravvivono le cellule che hanno un’affinità
(t/2= 4 gg), che producono IgM aumentata nei confronti dell’antigene. Inoltre, le cellule
e non formano cellule della eseguono anche lo scambio isotipico (cioè cambiano la natura
memoria (analogamente alle dell’anticorpo prodotto: da IgM a IgG, IgA, IgE). Da queste
cellule B attivate da antigeni Ti) cellule derivano: (i) plasmacellule a vita lunga (terminali), e (ii)
cellule B della memoria.
Le PLASMACELLULE A VITA LUNGA migrano (in Le CELLULE B DELLA MEMORIA (a vita lunga) hanno BCR
genere nel MO) e producono (anche per con un’affinità maggiore per l’antigene, un maggior
diversi mesi) anticorpi ad alta affinità. numero di molecole di adesione, e possono
funzionare da APC per cellule Th di memoria. Di
conseguenza, la risposta immunitaria secondaria è
molto più rapida ed efficace di quella primaria.Fab Struttura degli anticorpi: catene leggere (rosa) e
catene pesanti (azzurro).
Le regioni più chiare, costituite dai domini variabili,
interagiscono con l’antigene. Le regioni più scure
(domini costanti), sostengono le funzioni effettrici
degli anticorpi.
Fc
Funzioni effettrici degli anticorpi
neutralizzazione Alcuni virus, tossine batteriche, e veleni producono un danno legandosi alla
superficie cellulare. Un anticorpo neutralizzante impedisce fisicamente
all’agente patogeno di interagire con la cellula e di provocare un danno.
attivazione del complemento Se un agente patogeno è rivestito da anticorpi IgG o IgM, si avvia l’attivazione
(via classica) del complemento, con formazione di MAC e reazione infiammatoria.
opsonizzazione Gli anticorpi rivestono l’antigene e facilitano il riconoscimento dell’agente
patogeno da parte dei fagociti (che sono dotati di recettori FcR)
citotossicità cellulo-mediata Un agente patogeno troppo grande per essere fagocitato è ucciso da cellule con
anticorpo-dipendente (ADCC) capacità citotossica (NK, eosinofili) che possiedono recettori FcR.proprietà delle principali classi di anticorpi (isotipi) umani
IgM IgD IgG IgA IgE
catene pesanti μ δ γ α ε
% Ig circolanti 10La memoria immunitaria (cellule Th, Tc, e B)
Cellule Th e Tc
della memoria
meccanismo di formazione
▪ modello lineare: derivano da una (piccola) quota di cellule effettrici che resistono all’apoptosi.
▪ modello divergente: seguono una via maturativa diversa da quella delle cellule effettrici.
La risposta al riconoscimento antigenico è più veloce ed efficiente della risposta alle cellule naive, grazie a
varie caratteristiche fenotipiche:
▪ lunga sopravvivenza: diversamente dalle cellule effettrici, la sopravvivenza delle cellule della memoria
non dipende dal riconoscimento antigenico, ma è legata all’effetto di citochine come IL7 e IL15 che
aumentano l’espressione di proteine anti-apoptotiche.
▪ capacità di autorinnovamento (citochine?)
▪ modificazioni epigenetiche: accessibilità dei loci genici coinvolti nella risposta immunitaria
▪ dislocazione anatomica: le cellule della memoria possono localizzarsi nei tessuti periferici, nelle sedi di
attivazione della risposta immunitaria.
Cellule B della
memoria
▪ Derivano dalle cellule B che, sotto la guida di Th, hanno effettuato la maturazione dell’affinità
(ipermutazione somatica), e quindi sono in grado di riconoscere con molta più efficienza l’antigene che ha
determinato l’attivazione della corrispondente cellula naive.Mancata risposta del sistema adattativo ad un determinato antigene, causata da una
tolleranza immunitaria
precedente esposizione allo stesso.
Principi della tolleranza, e loro basi biologiche
Regola generale: I linfociti con BCR/TCR capace di riconoscere antigeni propri (autoreattivi) vengono:
gli antigeni self sono tollerati ▪ eliminati
▪ inattivati
▪ indotti a modificare la propria specificità (cellule B )
La tolleranza viene generata ▪ Tolleranza centrale: i linfociti autoreattivi vengono eliminati nel MO o nel timo.
negli organi linfoidi centrali ▪ Tolleranza periferica:
durante il processo di ▪ i linfociti autoreattivi vengono eliminati o resi incapaci di attivarsi in un
maturazione, e in quelli incontro successivo con l’antigene (anergia).
periferici. ▪ i linfociti Treg inibiscono attivamente i linfociti autoreattivi.
Alcuni antigeni self sono In alcune sedi, specifiche barriere anatomiche (santuari) sequestrano gli antigeni
nascosti al sistema self (occhio, testicolo).
immunitario
La tolleranza (periferica) può La presentazione di antigeni non-self in assenza di segnali di costimolazione può
essere indotta anche da indurre tolleranza periferica (microbi, alcuni tumori).
antigeni non-self
Rilevanza clinica della ▪ alterazioni dei meccanismi della tolleranza determinano malattie autoimmuni.
tolleranza ▪ i meccanismi della tolleranza possono essere sfruttati terapeuticamente ai fini
del contenimento di reazioni immunitarie eccessive.Sviluppo delle cellule T nel timo, e tolleranza centrale. Precursori della linea T arrivano nella corticale timica e iniziano il riarrangiamento dei geni TCR. Selezione positiva: sopravvivono solo le T immature CD4+CD8+ (doppio- positive) con recettori capaci di riconoscere MHC self sulle cellule epiteliali corticali. Selezione negativa: a livello della giunzione cortico-midollare, le cellule T sondano antigeni self pMHC I e pMHC II presentati da DC e MØ. Nel caso di riconoscimento ad alta affinità le cellule T muoiono per apoptosi. Il riconoscimento a bassa affinità del self, assieme alla repressione dell’espressione di CD4 o di CD8, produce cellule T naive CD4+ o CD8+ capaci di “tollerare” gli antigeni self, e di riconoscere antigeni non-self presentati dal MHC. Si ritiene che solo l’1% delle T superi i processi selettivi.
Tolleranza centrale e tolleranza periferica
Nella tolleranza centrale, il processo di selezione negativa nel timo elimina i linfociti immaturi che riconoscono con
forza l’antigene self presentato....
Ma da dove vengono gli antigeni self presentati dalle cellule del timo, e come vengono eliminati i
linfociti immaturi che li riconoscono?
Gli Ag self provengono:
▪ dalle proteine circolanti, internalizzate dalle DC del timo e presentate come pMHC classe II
▪ dalle stesse cellule del timo che hanno la specifica proprietà di presentare pMHC di classe I in cui
«p» deriva anche da proteine espresse usualmente in altre sedi dell’organismo (programma
trascrizionale AIRE, autoimmune regulator).
▪ I linfociti immaturi che riconoscono con forza l’antigene self muoiono per apoptosi.
Ma che succede nel caso che Ag self non
vengano presentati alle T immature, e
quindi T mature e capaci di riconoscere
Ag self (autoreattive) escono dal timo?Tolleranza periferica!
Anergia Se il TCR di una TCD4+ è stimolato in modo persistente (segnale 1) ma mancano
segnali di costimolazione, la TCD4+ diventa anergica (non responsiva nei confronti
dei segnali provenienti dal TCR).
Delezione (morte Le cellule T che riconoscono antigeni self con alta affinità (o che sono
cellulare) ripetutamente stimolati da Ag persistenti), muoiono per apoptosi in assenza di
segnali di costimolazione.
Inibizione da Treg ▪ Le cellule Treg nascono nel timo e hanno un TCR con affinità intermedia per Ag
self
▪ in alternativa, le Treg si formano in periferia incontrando antigeni self o non self
in assenza di attivazione dell’immunità innata.
▪ le Treg:
▪ inibiscono la capacità di presentazione dell’antigene delle DC (via CTLA-4)
▪ producono citochine immunosoppressive (TGFβ e IL10).Le cellule Treg: modello di funzionamento
Th naive con TCR Th naive con TCR Th naive con TCR ad
ad alta affinità per ad alta affinità per affinità intermedia
pMHC self pMHC non self per pMHC self (Treg)
Attivazione in Th Attivazione delle Treg
effettrici da parte a seguito dell’incontro
di mDC con pMHC self
Le Th effettrici Le Treg effettrici
agiscono riconoscendo inibiscono la funzione
pMHC non self delle Th effettrici
Quando pMHC non self è
Le Th effettrici inibiscono le Treg eliminato, le Th effettrici
fino a quando è presente pMHC rilasciano l’inibizione sulle Treg, e
non self. queste inibiscono le Th effettrici.IMMUNOLOGIA & IMMUNOPATOLOGIA
BENEFICI POTENZIALI DANNI
Analogamente a quanto
▪ Se la risposta
detto per
immunitaria non è
l’infiammazione, la
adeguatamente
risposta immunitaria
controllata e/o è
ottimizza l’eradicazione
diretta verso i tessuti
dei patogeni, ed è
propri è responsabile
controllata per non
di danno immuno-
provocare eccessivi
mediato.
danni ai tessuti
dell’ospite.
▪ Se la risposta immunitaria è
deficitaria, insorgono gravi
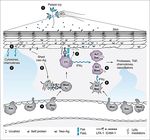
malattie (immunodeficienza).Il danno immuno-mediato: La risposta immunitaria è innescata o mantenuta in modo improprio
a) nei confronti di ANTIGENI MICROBICI
- reazioni eccessive o persistenza di antigeni microbici
-gli anticorpi, legandosi agli antigeni, possono dar luogo alla formazione di «complessi immuni» che si localizzano nei tessuti
e inducono infiammazione;
-le risposte cellulo-mediate nei confronti di antigeni persistenti danneggiano i tessuti e inducono infiammazione.
-reattività crociata: la risposta umorale/cellulare nei confronti di antigeni microbici colpisce anche antigeni dell’ospite.
b) nei confronti di ANTIGENI AMBIENTALI
Nel 20% della popolazione, c’è una predisposizione genetica a sviluppare una forte risposta immunitaria verso comuni
antigeni presenti nell’ambiente (pollini, acaro della polvere etc).
c) nei confronti di AUTOANTIGENI
una deficienza dei meccanismi di tolleranza è alla base di reazioni immunitarie contro cellule e tessuti del proprio stesso
organismo (malattie autoimmuni).
In tutte le condizioni sopra descritte, è difficile (o impossibile) eliminare gli antigeni
Le malattie associate a danno immuno-mediato tendono ad essere croniche (e debilitanti).
Componente fondamentale del quadro patologico è l’infiammazione cronica (MALATTIE
INFIAMMATORIE SU BASE IMMUNITARIA).Danno immuno-mediato: i meccanismi (1).
I meccanismi effettori finali dell’immunità adattativa sono quelli dell’immunità innata, e quindi il danno
immuno-mediato è conseguente ad un’attivazione inappropriata dei sistemi dell’immunità innata da
parte di....
anticorpi
Un anticorpo è in pratica una
molecola adattatrice che lega
l’antigene al recettore di una
cellula effettrice, che dirigerà la
sua risposta nei confronti del
bersaglio. La capacità di
attivare il complemento (IgM e
IgG) migliorerà la capacità di
identificazione del bersaglio.
I recettori FcR delle cellule dell’immunità innata hanno un ruolo centrale:*
▪ FcγR (recettore per la catena pesante γ delle IgG)
▪ classe ampia di recettori espressi su fagociti (PMN, MØ), piastrine, mastociti, eosinofili e NK.
▪ i complessi IgG- FcγR avviano un programma ampio (non univoco) di risposte cellulari che vanno dalla fagocitosi
(PMN e MØ), alla citotossicità (NK), all’aggregazione piastrinica e trombosi (piastrine).
▪ FcεR (recettore per la catena pesante ε delle IgE)
▪ recettori espressi su mastociti, basofili, ed eosinofili attivati.
▪ legano IgE monomeriche che -ingaggiate da antigeni multivalenti- avviano risposte effettrici (allergia).
*Si consideri che le cellule dell’immunità innata esprimono sia FcR attivatori che FcR inibitori, per cui la risposta
cellulare ad uno stimolo deriva in realtà dal bilancio dell’azione di recettori attivatori e recettori inibitori.Danno immuno-mediato: i meccanismi (2).
I meccanismi effettori finali dell’immunità adattativa sono quelli dell’immunità innata, e quindi il danno
immuno-mediato è conseguente ad un’attivazione inappropriata dei sistemi dell’immunità innata da
parte di....
cellule T le cellule T (in aggiunta agli anticorpi) possono provocare un danno tessutale:
▪ quando una T di memoria è esposta all’antigene, rilascia citochine e chemochine che attivano le
cellule endoteliali e reclutano e attivano cellule dell’immunità innata.
▪ Il danno tessutale può derivare dalle citochine prodotte dalle cellule effettrici (e quindi dalle
cellule dell’immunità innata da esse attivate), o dall’azione diretta di CTL.
▪ Th1: mediante la produzione di IFNγ attivano i macrofagi (attivazione classica), con
conseguente danno tessutale.
▪ Th2: mediante la produzione di IL4, IL5 ed eotassina, reclutano e attivano eosinofili, con
conseguente danno tessutale.
▪ Th17: producono IL17, che recluta e attiva PMN, con conseguente danno tessutale.
▪ Tc: differenziandosi in CTL possono determinare danno tessutale uccidendo direttamente
le cellule identificate come bersaglioIl danno immuno-mediato: REAZIONI DI IPERSENSIBILITÀ
«Ipersensibilità» è un termine generico che indica una risposta immunitaria adattativa eccessiva e
dannosa; le reazioni di ipersensibilità sono classificate in base ai meccanismi effettori implicati (ovvero
in base ai meccanismi prevalenti con cui si determina il danno).
reazioni di ipersensibilità tipo I-IV
tipo tipo I tipo II tipo III tipo IV
(altri nomi) (immediata, allergia) (da anticorpi) (da immunocomplessi) (ritardata, cellulo-mediata)
agente
IgE IgG o IgM IgG o IgM cellule T, macrofagi
effettore
insorgenza dei
< 1- 30 min 5-8 h 4-6 h 24-72 h
sintomi
meccanismo IgE legate sulla IgG o IgM legano Si formano cellule T effettrici
superficie di mastociti antigeni sulla immunocomplessi che producono IFNγ e (e altre
e basofili reagiscono superficie attivano il complemento; citochine) che iperattivano i
con allergeni e cellulare. la cellula attivazione dei fagociti; macrofagi.
determinano muore per produzione di mediatori
degranulazione. fagocitosi e/o per dell’infiammazione.
azione del MAC
e/o per ADCC.
esempi asma, febbre da
AR, LES (alcune
fieno, orticaria, anemia emolitica tubercolosi, lebbra.
forme)
allergie alimentari.
ADCC, citotossicità cellulo-mediata anticorpo-dipendente; AR, artrite reumatoide; LES, Lupus eritematosus sistemico.Ipersensibilità di tipo I
(ipersensibilità immediata, ipersensibilità IgE-mediata)
Gli allergeni (in genere proteine
Più nota come allergia, si determina in solubili) appartengono a sostanze più
grandi (pollini, forfora di animali )
soggetti che -per motivi ignoti- effettuano
un’intensa risposta Th2 con produzione di IgE
contro antigeni (detti allergeni) presenti Api m 1 veleno d’api
nell’ambiente e normalmente innocui per la Ara h 2 arachidi
maggior parte degli individui. (1)
Bet v 1 polline di betulla
Nei mastociti, le IgE determinano il rilascio Can f 1 peli di cane
dei mediatori responsabili delle
Der p 1 acaro della polvere
manifestazioni cliniche della reazione.
Pen a 1 gamberetti
manifestazioni cliniche delle reazioni di ipersensibilità di tipo I
▪ reazioni locali
▪ Cute: dermatite atopica (eczema); orticaria atopica
▪ Mucose: febbre da fieno, congiuntivite allergica, gastroenterite
allergica, asma bronchiale
▪ reazione sistemica: anafilassi (la reazione interessa l’intero organismo)
(1) La maggior parte degli individui produce anticorpi IgM, IgG o IgA nei confronti degli allergeni con cui viene in
contatto, rimuovendoli in modo asintomatico.Puoi anche leggere