ESMO 2020 - Carcinoma mammario triplo-negativo e recettori ormonali positivi in stadio precoce - Carcinoma mammario triplo-negativo e recettori ...
←
→
Trascrizione del contenuto della pagina
Se il tuo browser non visualizza correttamente la pagina, ti preghiamo di leggere il contenuto della pagina quaggiù
REPORT - Domenica 20 settembre 2020
ESMO 2020 - Carcinoma mammario triplo-negativo e recettori
ormonali positivi in stadio precoce
A cura di Benedetta Conte, U.O. Oncologia Medica 2, Ospedale Policlinico San Martino IRCCS, Genova
Domenica 20 settembre all’ESMO 2020 sono stati presentati gli studi che hanno implicazioni importanti
nel trattamento del carcinoma mammario triplo-negativo (TNBC) e recettori ormonali positivi (HR+) in
stadio precoce.
I risultati dello studio IMpassion031 hanno apportato ulteriori evidenze sull’efficacia della chemio-
immunoterapia come trattamento neoadiuvante del TNBC. Questo studio, di fase III in doppio cieco, ha
randomizzato 333 pazienti con TNBC e stadio clinico II-III, a ricevere in setting neoadiuvante 12 cicli di
nab-paclitaxel settimanale + atezolizumab/placebo bisettimanale alla dose di 840 mg, seguiti da 4 cicli
di doxorubicina e ciclofosfamide + atezolizumab/placebo bisettimanali, sempre alla dose di 840 mg.
Dopo la chirurgia, le pazienti allocate al braccio sperimentale hanno proseguito il mantenimento con
ulteriori 11 cicli trisettimanali di atezolizumab alla dose di 1200 mg.
Il disegno statistico iniziale prevedeva come unico endpoint primario la risposta completa patologica (pCR)
nella popolazione globale di studio. In seguito alla pubblicazione dei risultati dello studio IMpassion130,
che hanno mostrato un beneficio con atezolizumab solo nelle pazienti con TNBC metastatico PD-L1-
positivo (PD-L1+), lo studio è stato emendato per includere la pCR nelle pazienti PDL1+ come endpoint
co-primario. La positività di PD-L1 è stata definita sulla base del riscontro alla biopsia di un’espressione
di PD-L1 ³1% da parte dell’infiltrato immunitario peritumorale. La randomizzazione delle pazienti è stata
stratificata in base allo stadio di malattia (stadio II vs stadio III) e allo stato di PD-L1.
©Accademia Nazionale di MedicinaNello studio è stata arruolata solo una minoranza di pazienti con carcinoma mammario localmente
avanzato propriamente detto (stadio III, 23% delle pazienti arruolate), mentre la maggioranza (76%) aveva
un tumore di stadio II. Il 46% delle pazienti aveva un carcinoma mammario PD-L1+, mentre il 56% era PD-
L1-.
Nella popolazione generale, la pCR è risultata essere del 57,6% nel braccio con atezolizumab vs 41,1% nel
braccio di controllo, con un beneficio assoluto del 16,5%, statisticamente significativo (p=0,0044). Nella
popolazione PD-L1+ (46% della popolazione totale), la pCR è risultata del 68,8% nel braccio con
atezolizumab e del 49,3% nel braccio di controllo (beneficio assoluto: 19,5%, p=0,021). Nelle pazienti PD-
L1- (il 54% della popolazione totale), la pCR nel braccio con atezolizumab è risultata essere del 47,7 vs
34,4% nel braccio di controllo.
Il follow-up è ancora immaturo per osservare eventuali differenze significative negli outcomes di
sopravvivenza; tuttavia, sembra emergere un trend a favore del braccio con atezolizumab.
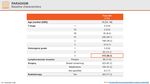
©Accademia Nazionale di MedicinaNella stessa sessione sono stati presentati i risultati dello studio PARADIGM, uno studio
osservazionale olandese che, utilizzando i dati del Netherlands Cancer Registry, ha analizzato la
correlazione tra prognosi a lungo termine e TIL (tumour infiltrating lymphocytes) in pazienti giovani con
TNBC non trattate con terapia sistemica (neo)adiuvante. Lo studio ha dimostrato che la stratificazione
prognostica delle pazienti sulla base dei TIL è in grado di identificare tre gruppi a rischio di ricaduta
differente. Le pazienti i cui tumori sono caratterizzati da un ampio infiltrato immunitario (TIL ³75%) hanno
un’ottima sopravvivenza anche in assenza di chemioterapia (neo)adiuvante (sopravvivenza globale (OS)
©Accademia Nazionale di Medicinaa 15 anni del 93%; confidence interval CI, 88–98%), mentre le pazienti con più bassa espressione di TIL (
I dati di questo studio confermano ancora una volta la necessità di includere i TIL tra i parametri
prognostici del TNBC. Gli autori concludono inoltre che questi risultati costituiscono evidenze importanti
per lo sviluppo di studi di de-escalation in pazienti giovani con TNBC con alta espressione di TIL.
Il carcinoma mammario HR+ è stato invece il protagonista indiscusso della seconda parte di questa
giornata di ESMO 2020. Per la prima volta sono stati presentati i dati di efficacia nel setting adiuvante
degli inibitori di CDK4/6, con esiti contrastanti.
Lo studio PALLAS ha randomizzato 5600 pazienti con carcinoma mammario HR+ operato, con stadio
patologico II-III, a ricevere la terapia endocrina adiuvante associata o meno a palbociclib per due anni. Il
tipo e la durata della terapia endocrina erano a discrezione dello sperimentatore. Lo switch da tamoxifene
a inibitore dell’aromatasi era consentito, e la soppressione ovarica era prevista per le pazienti in
premenopausa in trattamento con inibitore dell’aromatasi.
Endpoint primario dello studio era la sopravvivenza libera da malattia invasiva (iDFS). Endpoints secondari
erano sopravvivenza libera da carcinoma mammario, sopravvivenza libera da recidiva a distanza (dRFS),
sopravvivenza libera da recidiva loco-regionale e OS.
A un follow-up mediano di quasi 24 mesi, lo studio è risultato negativo: la iDFS è risultata essere
dell’88,2% nel braccio con palbociclib, e dell’88,5% nel braccio con sola terapia endocrina (HR=0,93, CI
0,76–1,15, p=0,51). Analogamente, non sono state riscontrate differenze statisticamente significative
in dRFS tra i due bracci di trattamento: HR=1,00, CI 0,79–1,27, p=0,99.
È importante sottolineare che una percentuale significativa di pazienti è andata incontro a una
sospensione del trattamento e/o a riduzione della dose previste dal protocollo a seguito di tossicità
ematologica (prevalentemente neutropenia G3), con un possibile effetto detrimentale sui dati di efficacia
dello studio.
©Accademia Nazionale di MedicinaLo studio MonarchE, presentato in sessione plenaria, ha arruolato un profilo di pazienti più ad alto rischio
rispetto allo studio PALLAS: erano eleggibili per lo studio solo le pazienti con almeno quattro linfonodi
ascellari metastatici, o da uno a tre linfonodi ascellari metastatici e con tumori ³5 cm, e/o di alto grado
(G3), e/o con un Ki-67 ³20%. Nello studio PALLAS le pazienti con almeno quattro linfonodi ascellari
metastatici rappresentavano il 38% della popolazione di studio vs il 59% nello studio MonarchE. Il
MonarchE ha randomizzato 5637 pazienti a ricevere la terapia endocrina adiuvante associata o meno ad
abemaciclib per due anni. Analogamente allo studio PALLAS, il tipo e la durata dell’endocrinoterapia
erano a discrezione dello sperimentatore.
©Accademia Nazionale di MedicinaEndpoint primario era la iDFS. Endpoints secondari erano la dRFS, l’OS, e la safety. I risultati presentati in
sessione plenaria a ESMO 2020 sono relativi all’analisi ad interim a due anni, e da considerarsi quindi
ancora immaturi.
Abemaciclib ha dimostrato di ridurre in maniera statisticamente significativa il rischio di iDFS a due anni
del 26% (HR=0,747, CI 0,59–0,93) con un beneficio assoluto del 3,5%. Analogamente, il rischio di dRFS a
due anni è risultato significativamente ridotto nel braccio con abemaciclib: HR=0,71 (CI 0,55–0,92), con
beneficio assoluto del 3,3%.
©Accademia Nazionale di MedicinaIn sede di congresso sono state discusse le possibili motivazioni del differente esito degli studi PALLAS
e MonarchE:
- differenza nel disegno dei due studi. Rispetto allo studio PALLAS, lo studio MonarchE ha
arruolato pazienti a più alto rischio di ricaduta, e ciò ha permesso di osservare un beneficio
significativo dall’aggiunta dell’inibitore di CDK4/6;
- differenze nell’aderenza alla terapia con l’inibitore di CDK4/6. Nonostante il buon profilo di
tollerabilità di palbociclib, il 42% delle pazienti arruolate nello studio PALLAS ha interrotto e/o
ridotto la dose del farmaco come previsto dal protocollo, vs il 16% delle pazienti nello studio
MonarchE;
- differenza nel profilo di efficacia dei due farmaci. La schedula di somministrazione continua di
abemaciclib potrebbe essere più efficace rispetto all’assunzione intermittente. Inoltre, i due
farmaci hanno selettività diversa per CDK4 e CDK6.
Per quanto incoraggianti, i dati di efficacia di abemaciclib a 24 mesi sono ancora preliminari. È
necessaria la pubblicazione dei dati definitivi per confermare l’efficacia nel ridurre il rischio di ricaduta
e per osservare un eventuale beneficio in sopravvivenza.
©Accademia Nazionale di MedicinaPuoi anche leggere