Aspetti innovativi di identificazione e trattamento delle infezioni da Clostridium difficile - Paolo Lanzafame U.O. Microbiologia e Virologia ...
←
→
Trascrizione del contenuto della pagina
Se il tuo browser non visualizza correttamente la pagina, ti preghiamo di leggere il contenuto della pagina quaggiù
Aspetti innovativi di
identificazione e trattamento delle
infezioni da Clostridium difficile
Paolo Lanzafame
U.O. Microbiologia e Virologia - Ospedale di Trento!! Batterio Sporigeno Gram +
!! !"#$%#&'()*(&%$+#*%,-%#.(#.(%''+%#!"#$%&'#()#&%/(+)0#'+-(.+)/(%$(#12-&+.%$(3#4563+7*889
!! Sono stati identificati due ceppi di C. difficile: tossigenico e non tossigenico, solo
il ceppo tossigenico è responsabile di C. difficile-associated disease (CDAD).
!! C. difficile causa colite pseudomembranosa, megacolon tossico, sepsi,
perforazione con conseguente pancolectomia e in alcuni casi decesso del
paziente.
!! C. difficile è responsabile per il 15-20% di diarrea associata a terapia antibiotica
e al 100% di casi di colite pseudomembranosa.
!! Il tasso di mortalità per CDAD negli USA è incrementato da 5.7 per milione di
persone nel 1999 a 23.7 per milione nel 2004.
!! La comparsa di infezione fulminante associata a C.difficile è sempre più comune.
Presumibilmente associata alla comparsa di ceppi ipervirulenti con un marcato
incremento di morbidità e mortalità in particolare durante le epidemie.Epidemiologia
L’epidemiologia in Europa si
caratterizza per tre aspetti distintivi:
1.!una diffusione in senso nord-sud;
2.!la maggiore incidenza ha interessato
paesi culturalmente più avanzati per
quanto attiene il controllo delle
infezioni nosocomiali;
3.! il ruolo del ceppo NAP1/BI/027
appare ancora limitato. L’epidemia
europea ha, infatti, avuto inizio nei
Paesi settentrionali (Paesi Bassi,
Svezia, Gran Bretagna), per poi
coinvolgere le nazioni continentali
(Belgio, Germania, Austria, Francia) e,
da ultimo, gli stati mediterranei
(Grecia e Spagna).Fattori di rischio !!Ospedalizzazione con tempi prolungati !!Profilassi e terapia antibiotica, soprattutto se combinata e protratta (clindamicina, ampicillina, cefalosporine 3^, fluorochinolonici) !!età (>65 anni)
!! I fattori di virulenza primari sono tossina A and B
!! Responsabili di infiammazione , secrezione mucosa e danno a
livello delle mucose intestinali che porta a diarrea e colite.
!! Tossina A: attacca neutrofili e monociti
!! Tossina B: distrugge le cellule epiteliali
!! Solo il ceppo tossigenico di C.difficile è responsabile della
patologia:
!! Tossina A (tcdA): non sempre presente
!! Tossina B (tcdB): sempre presente nel C.difficile tossigenico
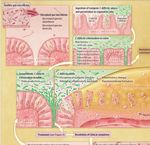
!! Tossina binaria: può essere o non essere presente.From: Bagdasarian N. et al - Diagnosis and Treatment of Clostridium difficile in Adults:!!A Systematic Review
JAMA. 2015;313(4):398-408
Steps in the
Pathogenesis of
Clostridium difficile
Infection and Possible
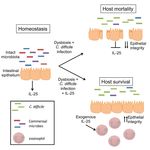
Treatment OutcomesFrom: Buonomo E L. et al - Microbiota-Regulated IL-25 Increases Eosinophil Number to Provide Protection
during Clostridium difficile Infection - Cell Reports 16, 432–443, July 12, 2016
Clostridium difficile infection
(CDI):
Host susceptibility and the
severity of infection are
influenced by disruption of the
microbiota and the immune
response. However, how the
microbiota regulate immune
responses to mediate CDI
outcome remains unclear.
Intestinal IL-25 was
suppressed during CDI in
humans and mice. Restoration
of IL-25 reduced CDI-
associated mortality and tissue
pathology even though
equivalent levels of C. difficile
bacteria and toxin remained in
the gut. IL-25 protection
was mediated by gut
eosinophils, as demonstrated
by an increase in intestinal
eosinophils and a loss of IL-25
protection upon eosinophil
depletion.
These findings support a
mechanism whereby the
induction of IL-25-mediated
eosinophilia can reduce host
mortality during active CDI.!! 5-6% di C. difficile isolato produce la tossina binaria
!! E’ responsabile di conferire una maggiore virulenza (Barbut t
al., JMM, 2005; Terhes et al., JCM, 2004)
!! Necessità di un trattamento più rapido e aggressivo
rispetto al ceppo positivo solo per le Tossine A/B
!! Il ceppo positivo alla tossina binaria è associato sia ad
infezioni nosocomiali che acquisite in ambito comunitario.!! Delezione del gene regolatore tcdC
!! tcdC è il gene che controlla la produzione della Tossina
A&B
!! Se il ceppo di C. difficile perde il gene tcdC, incrementa
di 16 volte la produzione di Tossina A e di 23 volte la
produzione di Tossina B.
!! I ceppi di C. difficile con delezione del gene
regolatore sono molto più virulenti:
!! NAP1/027/BI strain produce più tossina; la
sintomatologia clinica risulta essere molto più severa.!! Il ceppo epidemico NAP1/027/BI è positivo alla tossina B, alla tossina binaria e presenta delezione del gene regolatore tcdC. !! Più resistente ai fluorochinoloni e alle cefalosporine di IIIa generazione. !! Per il ceppo ipervirulento la terapia deve essere iniziata il più rapidamente possibile a causa dell’alto tasso di mortalità (50%).
A chi effettuare i test ????
"!Tutti i pazienti con diarrea insorta dopo 48 ore dal ricovero
"!Pazienti con diarrea al ricovero o insorta entro le prime 48
ore dal ricovero se:
"!Dimessi da un ospedale da non più di 4 settimane
"!In terapia antibiotica
"!Con diarrea severa
"!Non eseguire il test a pazienti asintomatici
"!Non eseguire il test per follow-up dopo terapia se
paziente asintomatico nè per dimissione o
trasferimentoDiagnosi: Come???
Diagnosis of Clostridium difficile Infection: an Ongoing Conundrum for Clinicians and
for Clinical Laboratories.
Carey-Ann D. Burnham
Clostridium difficile: valore clinico della
diagnosi di laboratorio
Il clinico è alla ricerca di un test rapido, sensibile e specifico che
permetta il trattamento appropriato e l’isolamento del paziente
per limitare rapidamente la trasmissione del patogeno.
Abilità nel riconoscere i ceppi iper-tossigenici di C.difficile resistenti
alle terapie antibiotiche standard.Dove????
Non su feci formate
Il tampone rettale non è idoneo•! Metodi non microbiologici:
•! Sintomatologia clinica
•! Endoscopia
•! Identificazione del C. difficile :
•! Coltura
•! Glutamate dehydrogenase GDH
•! Identificazione della Tossina
•! Ricerca della Tossina B
•! EIA
•! Test di citotossicità
•! Geni della Tossina (PCR)
!From: Bagdasarian N. et al - Diagnosis and Treatment of Clostridium difficile in Adults:!!A Systematic Review
JAMA. 2015;313(4):398-408
Diagnostic Tests for Toxigenic
Clostridium difficile19
La ricerca della tossina (EIA) stand-alone è
inadeguata.
Bassa sensibilità basso valore predittivo negativo
La ricerca del GDH (EIA) ha una migliore sensibilità, è più
rapida e con costi inferiori.
La ricerca del GDH ha un alto valore predittivo negativo
Tuttavia non distingue tra ceppi tossigenici e non
tossigenici
Deve essere utilizzato in combinazione con la ricerca della
tossina
Gelone et al Late Breaker Abstract SHEA Ann Mtg Chicago 200620 countries participating
22
23
24
From: Bagdasarian N. et al - Diagnosis and Treatment of Clostridium difficile in Adults:!!A Systematic Review
JAMA. 2015;313(4):398-408
Sample Multistep Algorithm for Rapid Diagnosis of Clostridium difficile Infection Abbreviations: EIA, enzyme immunoassay; GDH,
glutamate dehydrogenase; PCR, polymerase chain reaction.
aToxin-positive (+) indicates presence of either Toxin A or Toxin B when a combined test is performed, as in this example. Toxin-
negative (") indicates that neither Toxin A nor B is present.(1)
GDH-Screen 3 Algoritmi diagnostici
C.diff GDH
Pos
Neg
(2)
GDH-Toxin A/B combinati
C diff ToxA/B
C.Diff Tox A/B
C diff GDH
Uno positivo
Pos Uno negativo
Pos Neg
Neg
entrambi
NAATS/Coltura entrambi
tossigenica C.diff
(3) Pos
NAATS/Coltura
Neg
NAAT stand alone test tossigenica C.diff
Pos Neg
NAATS C.diff
Pos Neg Pos Neg27
28
29
NAAT
NON per pazienti asintomatici
Saggi positivi dopo il trattamento non sono indice di ricaduta
Non idonei per il follow-up terapeutico (No“test of cure”)
Possono essere utilizzati stand-alone
i saggi molecolari ci aiutano
•! Gestione dei pazienti con forte
sospetto clinico ma con
risultato “C.difficile Negativo”
•! Sono necessari più test
diagnostici per confermare
C.difficile
l’infezione•!m igliore uso delle risorse di laboratorio
•!appropriate misure di prevenzione della infezione
•!adeguato trattamentoFrom: Bagdasarian N. et al - Diagnosis and Treatment of Clostridium difficile in Adults:!!A Systematic Review JAMA. 2015;313(4):398-408
32
From: Bagdasarian N. et al - Diagnosis and Treatment of Clostridium difficile in Adults:!!A Systematic Review
JAMA. 2015;313(4):398-408
CDI Classification Based on Disease SeverityFrom: Bagdasarian N. et al - Diagnosis and Treatment of Clostridium difficile in Adults:!!A Systematic Review
JAMA. 2015;313(4):398-408
Possible Approach for
the Treatment of
Clostridium difficile
Infection:
Suggested approach for
Clostridium difficile (CDI)
treatment according to
disease severity based on
current guidelines, recent
reviews and meta-analyses
of fecal microbiota
transplantation, and
randomized controlled
trials of fidaxomicin. This
approach is not validated.
There are no data
supporting the use of
fidaxomicin for complicated
CDI.
bTreatment response is
defined by clinical
improvement in diarrhea or
other signs of infection.
Response may require 3 to
5 days after starting
therapy, but therapy
escalation can be
considered sooner based
on disease severity.
cIndicates that costs are
substantially higher.
dDuration of therapy
depends on treatment
response.
eConsider postinfectious
irritable bowel syndrome
rather than recurrent CDI
for mild symptoms.NUOVE PROSPETTIVE TERAPEUTICHE •!Nuovi antibiotici •!Sostanze chelanti le tossine •!Agenti immunomodulatori •!Probiotici e trapianto fecale
!! !La fidaxomicina è un antibiotico di nuova generazione appartenente alla
classe chiamata a “narrow band” cioè a ristretto spettro d’azione. E’ un
antibiotico macrociclico non sistemico, naturale prodotto da
Dactylosporangium aurantiacum, il cui spettro d’azione include batteri gram
positivi aerobi e anaerobi (significativa concentrazione fecale).
!! La ramoplanina è un antibiotico lipoglicopeptidico che si è dimostrato attivo
verso batteri gram positivi sia aerobi che anaerobi esplicando la propria
attività antibatterica bloccando la sintesi del peptidoglicano. È stata
sviluppata per la terapia delle infezioni intestinali poiché raggiunge
concentrazioni molto elevate a livello fecale.
!! Strutturalmente simile alla vancomicina, la!teicoplanina!è un glicopeptide non
assorbibile che ha dimostrato attività contro C. difficile con delle MIC inferiori
a quelle della vancomicina stessa(tasso di cura 96% e tasso di recidive 7%)
!! Case reports riportano una buona efficacia della tigeciclina per CDI severa o
ricorrente. Tuttavia il ruolo della tigeciclina non è ancora chiaro.
!! Trials di fase 3 sono in corso per surotomicina and cadazolid.Sostanze chelanti le tossine Molecole come la colestiramina e il colestipol sono state sviluppate per la capacità di chelaggio delle tossine in sede endoluminale. Sono riportati casi di pazienti sia adulti che pediatrici che, dopo numerose recidive trattate con agenti tradizionali, hanno finalmente risposto a questo trattamento. Tuttavia i dati di trial randomizzati dimostrano che questi polimeri anionici non assorbibili non sono efficaci per CDI. Il tolevamer e un polimero anionico che lega sia la tossina A che B. Tuttavia studi recenti hanno dimostrato un’inferiorità netta rispetto a vancomicina e metronidazolo . Inoltre tali polimeri possono chelare anche altre sostanze come la vancomicina e non dovrebbero essere mai somministrati in contemporanea con altre terapie
!! La risposta anticorpale alla tossina A è in grado di proteggere dalle ricorrenze di CDI.
Un vaccino per C.difficile è in fase di sviluppo sia per l’infezione primaria che per le
ricorrenze . Pool di immunoglobuline neutralizza in vitro le tossine di C. difficile ma
!! Ci sono dati limitati riguardo al possibile utilizzo per via endovenosa nelle forme
ricorrenti ed il ruolo della risposta immunitaria rimane ancora non del tutto chiarito
!! Anche l’immunoterapia è stata a lungo studiata per valutare eventuali applicazioni
nella gestione della CDI.
!! In uno studio randomizzato, a doppio cieco, vs. placebo, Ab monoclonali umani verso
la tossina A (CDA1) e verso la tossina B (CDB1), in combinazione con la terapia
standard, hanno dimostrato una minore % di ricorrenze(7%vs 25%).
!! Studi di fase 3 stanno valutando altri 2 Ab monoclonali per la prevenzione delle
ricorrenze in associazione a terapia standard:
-! MK-3415 contro la tossina A
-! MK-6072 contro la tossina BProbiotici e trapianto fecale
L’utilizzo di probiotici è, da sempre, molto controverso: essi
agiscono come mezzo per restaurare la normale flora
microbica intestinale e in tal modo, teoricamente, prevenire
CDI. Vengono commercialmente utilizzati ceppi di batteri:
Lactobacillus rhamnosus GG e L. acidiphilus,
Bifidobacterium e del lievito Saccharomyces boulardii, ma la
loro efficacia è discutibile.
Solo S. boulardii in uno studio controllato vs placebo ha
dimostrato una riduzione significativa rispetto al placebo (9.4
vs 31%) delle recidive nei soggetti in cui era associato alla
vancomicina.
Recenti case reports hanno evidenziato che Kefyr, un
probiotico derivato dal latte fermentato, in associazione a
terapia standard riduce il numero delle ricorrenze
È stato osservato che il colostro umano possiede un’attività neutralizzante nei confronti delle
tossine A e B e questo può essere uno dei motivi per i quali i neonati sono spesso colonizzati
da clostridi senza tuttavia sviluppare la patologia.Mark A. Miller, uno dei maggiori esperti dell’epidemia di C.difficile
sostenuta da ceppi NAP1 manifestatasi all’inizio del decennio in
Quebec, ha definito il trapianto di feci (batterioterapia fecale)
attraverso un sondino nasogastrico come “l’approccio che nessuno
vuole fare pur essendo quello migliore e che non fallisce mai”. Il
trapianto viene eseguito prelevando un campione fecale da un
parente stretto o, se non disponibile, da un altro familiare o da
donatore sano (screening donatori problematico)
In un recente studio 20 pazienti con
ricorrenze di CDI non rispondenti al
trattamento standard sono stati trattati
con capsule di estratti fecali congelati ed
hanno presentato il 90% di risposta dopo
1 o 2 trattamenti
Reports aneddotici riportano l’utilizzo del
trapianto fecale anche nel trattamento di
CDI complicate, di ileo e del megacolon
Therapeutic Advances in GastroenterologyReview. Fecal microbiota transplantation
in relapsing Clostridium difficile infection Faith Rohlke and Neil Stollman.
Microbiome2015US FDA considera il trapianto fecale ancora sotto esame Poiché la disponibilità del paziente ad accettare questo tipo di approccio può, in ogni caso, rappresentare un limite, l’indicazione al trapianto dovrebbe essere valutata nei casi severi refrattari alle terapie convenzionali.
Smits, W. K. et al. (2016) Clostridium difficile infection Nat. Rev. Dis. Primers doi:10.1038/nrdp.2016.20
Grazie per l’attenzione
43Puoi anche leggere