B Foto-ossidazione e termo-ossidazione
←
→
Trascrizione del contenuto della pagina
Se il tuo browser non visualizza correttamente la pagina, ti preghiamo di leggere il contenuto della pagina quaggiù
B ) Foto-ossidazione e termo-ossidazione
La foto-ossidazione e la termo-ossidazione sono processi degradativi
provocati dall’azione combinata di luce ed ossigeno (foto-ossidazione) e
di calore ed ossigeno (termo-ossidazione).
Al fine di una migliore comprensione dei due fenomeni conviene ana-
lizzare, preliminarmente, i meccanismi indotti dall’azione della sola luce
(degradazione fotochimica) e del solo calore (degradazione termica), in
assenza di ossigeno.
B1 ) Degradazione fotochimica
Lo spettro elettromagnetico è costituito da radiazioni le cui lunghezze
d’onda () vanno da quelle delle onde radio ( > 106 nm) a quelle dei
raggi cosmici ( 10-4 nm) (figure 28 e 29) [20, 21].
Come traspare dalla figura 29 lo spettro visibile comprende radiazioni
con lunghezze d’onda tra 400 nm e 750 nm. La luce, nell’ambito di que-
sto intervallo, assume una colorazione diversa; in particolare all’aumen-
tare di
«si passa dal colore violetto (420 nm) fino ad arrivare al rosso (650 nm) pas-
sando attraverso tutte le tonalità intermedie di transizione (indaco, azzurro,
verde, giallo ed arancione)» (figura 30) [22].
Secondo la teoria corpuscolare della luce, sviluppata da Einstein ed
Altri, un fascio di luce si comporta come un flusso di particelle, fotoni,
ognuna delle quali ha un’energia E il cui valore è collegato alla frequenza
e alla lunghezza d’onda mediante la seguente relazione fondamentale:
E = h = h c / (8)
dove h è la costante di Planck e c è la velocità della luce.
Quando un fascio di fotoni investe un corpo materiale le molecole (o
atomi) costituenti, in determinate condizioni, interagiscono con le radia-
zioni incidenti e, assorbendo quanti energetici (E = h ), passano, da uno
stato fondamentale caratterizzato da una configurazione elettronica a
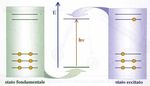
bassa energia, a stati eccitati a più elevata energia. Come illustrato sche-
maticamente nella figura 31, queste transizioni avvengono solo se l’ener-
gia della radiazione incidente è uguale alla differenza tra l’energia dello
stato eccitato e quella dello stato fondamentale.
Le molecole che si trovano in uno stato eccitato sono instabili e, per-
103Fig. 28: Le varie componenti e grandezze che caratterizzano le onde elettromagnetiche [20].
Fig. 29: Spettro elettromagnetico (la lunghezza d’onda è espressa in nm (nm = 1 milionesimo di
millimetro). Nella regione inferiore della figura, la parte visibile dello spettro è disaggregato
nelle varie onde componenti. L’energia associata alle radiazioni elettromagnetiche è tanto più
elevata quanto minore è la lunghezza d’onda [21].
tanto, tendono a disattivarsi attraverso processi di diseccitazione i più
importanti dei quali sono schematicamente indicati nella figura 32 [20].
I processi di disattivazione che riportano le molecole eccitate (A*) nello
stato fondamentale (A) attraverso la reazione A* A, che non prevede
fenomeni di trasformazione chimica, sono definiti fotofisici. Questi proces-
si possono avvenire per dissipazione di calore oppure attraverso l’emissio-
ne di quanti di luce h (fenomeno della luminescenza, che, a sua volta, a
104Fig. 30: Lo spettro visibile con colori associati alle varie onde elettromagnetiche che lo com-
pongono [22].
Fig. 31: Processo di assorbimento delle radiazioni luminose (schematico) [20].
105Fig. 32: I principali processi di disattivazione di uno stato elettricamente eccitato [20].
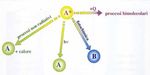
Fig. 33: Processi bimolecolari di spegnimento di uno stato eccitato [20].
seconda della velocità, dà luogo alla fluorescenza o alla fosforescenza).
Un terzo processo di diseccitazione, denominato fotochimico, si carat-
terizza per il fatto che il surplus di energia relativo allo stato eccitato
viene utilizzato nella reazione unimolecolare attraverso cui la molecola
eccitata A* viene trasformata in una molecola diversa (B) che si viene a
trovare nel suo stato fondamentale (A* B).
I fenomeni di fotoisomerizzazione cis trans degli alcheni sono clas-
sici esempi di transizione fotochimica unimolecolare.
La molecola eccitata A* può disattivarsi anche attraverso processi
bimolecolari, detti di spegnimento, trasferendo elettroni o energia ad
un’altra specie molecolare (vedasi figura 33) [20].
Come si deduce dal confronto dei diagrammi riportati nella figura 34,
106a) b)
Fig. 34: Distribuzione dell’intensità delle radiazioni solari in funzione della lunghezza d’onda:
a) spettro solare fuori dell’atmosfera terrestre; b) spettro solare in estate alle ore 12 nella città di
Washington D. C. (USA) [23].
le radiazioni solari aventi lunghezza d’onda inferiori a ~ 290 nm sono
assorbite totalmente dallo strato di ozono presente nell’atmosfera.
Pertanto, tenendo conto del fatto che le radiazioni ultraviolette hanno
lunghezza d’onda che varia tra i 100 e i 380 nm, è possibile concludere
che solo una frazione di queste ultime ha la capacità di investire la crosta
terrestre [23].
Dai diagrammi della figura 35 si ricava, inoltre, che la distribuzione
107a) b)
Fig. 35: Dipendenza dell’intensità delle radiazioni UV (< 313 nm):
a) dall’ora del giorno;
b) dal mese dell’anno [23].
108Tabella 2
Energie medie di legami chimici covalenti a 298K (in kJ/mole).
Legami Energie Legami Energie Legami Energie Legami Energie
C-S 273 Si-Si 226 P-N 200 C=C 612
C-Br 280 Si-H 319 P-C 264 C=N 617
C-N 307 Si-O 432 P-H 322 C=O 732
C-Si 328 N-H 391 P-O 360
C-Cl 340 O-H 464
C-C 349
C-O 361
C-H 416
C-F 485
dell’intensità relativa alle radiazioni ultraviolette (< 313 nm) dipende da
una serie di fattori: altitudine; latitudine, ora del giorno, stagione dell’an-
no e condizioni locali del tempo [23, 24].
L’energia dei fotoni delle radiazioni UV è sufficientemente elevata per
provocare la rottura di molti dei legami covalenti presenti lungo le
macromolecole di polimeri sintetici e naturali le cui energie medie (a 298
K; espresse in KJ mole-1) sono riportate nella tabella 2 [21].
Per degradazione fotochimica deve intendersi l’insieme di processi che,
a seguito di interazione con radiazioni luminose, comportano la modifica-
zione chimica (reazione fotochimica) di una sostanza colpita da fotoni.
È stato ampiamente dimostrato che le reazioni fotochimiche possono
avvenire solo se le molecole costituenti hanno la capacità di assorbire,
mediante un processo fotofisico, le radiazioni luminose [25].
Affinché in un polimero si verifichino reazioni fotochimiche è necessa-
ria la presenza, lungo la catena macromolecolare, di speciali gruppi, detti
cromofori, i quali hanno la capacità di assorbire quanti di luce passando
in uno stato elettronicamente eccitato. Successivamente l’energia assor-
bita a livello elettronico viene dissipata attraverso uno dei processi
discussi e già illustrati nelle figure 32 e 33.
La struttura chimica di alcuni dei più comuni gruppi cromofori presen-
109Tabella 3
Alcuni dei più comuni gruppi cromofori presenti in molecole organiche
ti in molecole e macromolecole organiche, sintetiche e naturali, è ripor-
tata nella tabella 3.
In alcune circostanze la presenza contemporanea di gruppi cromofori
diversi esalta l’attitudine di una molecola ad assorbire, mediante proces-
si fotofisici, radiazioni elettromagnetiche.
Questo caso si verifica in strutture molecolari del tipo qui di seguito
110delineate:
(a)
(b)
dove in molecole con insaturazioni coniugate [(doppi legami C=C (con
legami e ) si alternano a legami semplici C—C (legami vengono
inseriti dei gruppi aldeidici e/o chetonici.
Nei sistemi cromofori di cui sopra gli elettroni possono essere facil-
mente eccitati dalle radiazioni visibili. Gli elettroni di un legame
(C—H, C—C, C—O) richiedono, invece, una maggiore energia di atti-
vazione e quindi radiazioni a più bassa lunghezza d’onda e cioè quelle
che fanno parte delle regioni dell’ultravioletto (vedasi figura 29).
La presenza di gruppi e/o sistemi cromofori lungo le macromolecole di
una fibra tessile rende quest’ultima
«light sensitive because these groups absorb radiation in both the visibile
region and ultraviolet regions close to the visibile» [26].
Il processo di fotodegradazione delle fibre tessili prevede l’assorbi-
mento di fotoni da parte degli elettroni che partecipano ai legami chimi-
ci i quali passano in una configurazione eccitata.
A seguito di questa transizione e attraverso reazioni fotochimiche pri-
marie, la molecola eccitata viene dissociata in radicali.
«Il comportamento dei polimeri alla fotodegradazione è di solito il risultato
delle reazioni dei radicali creatisi dal processo fotochimico primario che
possono portare a scissioni della catena, reticolazioni, formazione di gruppi
insaturi ed eliminazione di gruppi sostituenti con formazione di composti
volatili» [27].
Durante la sintesi e la lavorazione può capitare che nella massa del
polimero restino incorporati composti estranei o additivi (ad esempio:
residui catalitici, tracce di idroperossido, monomeri contenenti gruppi
carbonilici, coloranti, mordenti, pigmenti, additivi utili alla lavorazione,
111Tabella 4
Il processo di fotodegradazione scomposto nelle sue varie fasi
112ecc.). Alcune di queste sostanze hanno la capacità di assorbire radiazioni
UV e di trasferire l’eccesso di energia alle molecole di polimero con for-
mazione di radicali i quali ultimi possono dare luogo ad una serie di pro-
cessi che portano alla fotodegradazione delle macromolecole.
Le fasi relative ad un processo di degradazione fotochimica, così come
descritte da J. C. McNeill, sono illustrate nella tabella 4 [25].
Il tipo di reazione a cui può dare luogo il macroradicale (R*) (fase 4, in
tabella 4) dipende, in generale, da una serie di fattori, i più importanti dei
quali sono:
- la temperatura di transizione vetrosa della fase amorfa della
fibra;
- la struttura chimica dell’unità ripetitiva delle macromolecole
costituenti;
- la presenza o l’assenza di atomi di idrogeno terziari che si ripe-
tono lungo la catena macromolecolare.
Al di sotto della temperatura di transizione vetrosa il processo di
«depropagation to monomer (fase 4-d in tabella 4; n.d.A.), which is an
important degradation reaction in some polymers at elevated temperatures,
cannot occur following chain scission induced photolytically, because when
the polymer is in the glassy state the propagation – depropagation equili-
brium cannot be driven to the right by the removal of monomer (vedasi rea-
zione sotto riportata; n. d. A)» [25].
La struttura molecolare dell’unità ripetitiva gioca un ruolo fondamen-
tale sui meccanismi di fotodegradazione . Ad esempio è stato osservato
che in polimeri con unità ripetitive senza atomi di idrogeno terziari,
la fotolisi provoca un abbassamento del peso molecolare a seguito di
reazioni di scissione delle macromolecole.
Nel caso di unità ripetitiva del tipo -CH2-CHX- allora l’effetto princi-
pale indotto dall’azione dei raggi ultravioletti è quello di provocare delle
reticolazioni.
È bene precisare che in entrambi i casi è essenziale, affinché si verifi-
113chino le reazioni fotochimiche sopra delineate, la presenza di gruppi cro-
mofori [25].
Le proprietà ultime di un polimero sottoposto ad attacco fotochimico
dipenderanno dal meccanismo molecolare secondo cui è evoluta la
degradazione. Se è prevalso il meccanismo di scissione delle macromo-
lecole si osserverà un decadimento delle caratteristiche fisico-meccani-
che a cui si accompagnerà un’aumentata solubilità, dovuta quest’ultima
al fatto che il peso molecolare medio è drasticamente ridotto. Al contra-
rio, nel caso che dovessero predominare reazioni di reticolazioni il mate-
riale presenterà una accentuata resistenza alla solubilizzazione e una
minor flessibilità.
114B2 ) Degradazione termica
Le fibre tessili ad alte temperature subiscono un processo di deteriora-
mento dovuto all’assorbimento di calore.
La stabilità termica di un polimero (sia esso naturale che sintetico)
dipende da una serie di fattori i più importanti dei quali sono:
- costituzione e configurazione molecolare dell’unità ripetitiva;
- legami secondari (per esempio ad idrogeno) di tipo intra e inter-
molecolare;
- grado di cristallinità;
- temperatura di fusione e di transizione vetrosa;
- presenza o meno di impurezze;
- massa molecolare;
- morfologia (sferulitica-isotropa, fibrosa-anisotropa);
- tipo di interconnessione tra fasi cristalline e fasi amorfe e strut-
tura delle zone di transizione;
- rigidità delle macromolecole e loro modo di impacchettarsi nella
fase cristallina [10-16].
La stabilità termica o resistenza termica (ST) di un polimero viene
comunemente così definita:
«la temperatura massima alla quale un polimero può essere riscaldato senza
che esso subisca modificazioni chimiche irreversibili» [27].
Normalmente la ST viene identificata con la temperatura alla quale un
polimero subisce una perdita, per effetto del calore, del 15% in peso (in
azoto e con una velocità di riscaldamento pari a 10 °C/min). La ST di
alcuni polimeri è riportata, a titolo esemplificativo, nella figura 36 [25].
Nel caso delle fibre tessili naturali è stato possibile stabilire la seguen-
te scala di resistenza alla termo - degradazione:
LINO > COTONE > LANA > SETA
dalla quale si deduce che le fibre proteiche (seta e lana) sono più sensi-
bili alla termo-decomposizione di quelle cellulosiche (lino e cotone) [28].
Le macromolecole delle fibre tessili naturali si caratterizzano per la pre-
senza lungo le loro catene di legami chimici covalenti (C-C, C-H, C-N,
C-O, ecc.) i quali hanno una energia di dissociazione che, come riporta-
to nella tabella 2, varia da 273 a 732 KJmole –1.
Tali legami tra i 150 °C e i 500 °C, a seconda degli atomi coinvolti, per
115Fig. 36: Stabilità termica relativa ad alcuni polimeri di più largo impiego. Essa viene misurata
dalla temperatura alla quale, in atmosfera di azoto e con una velocità di riscaldamento pari a 10
°C / min, si verifica il 15% di perdita di peso [25].
effetto del calore assorbito subiscono un processo di scissione denomi-
nato termolisi (in analogia alla fotolisi) che determina una serie di rea-
zioni che portano alla emissione di prodotti volatili a basso peso moleco-
lare e alla demolizione del polimero con perdita delle sue caratteristiche
fisico-meccaniche.
In assenza di ossigeno la degradazione termica può avvenire secondo
due meccanismi diversi:
a) reazioni che coinvolgono la catena polimerica (depolimerizzazione);
b) reazioni che coinvolgono i sostituenti laterali.
- Depolimerizzazione
«This name (la depolimerizzazione indotta da degradazione termica; n.d.A.)
can be applied to processes in which the chain breaks at same points, leading
to reactions in which the products all have essentially the same composition
as the repeat structure but may consist of relatively small molecules such as
monomer, dimer, trimer or chain fragments which are similar to the original
polymer or copolymer structure, but of much shorter chain length» [25].
Lo schema della depolimerizzazione è illustrato nella tabella 5.
A titolo esemplificativo nella figura 37 sono riportate le reazioni di
depolimerizzazione del polimetilmetacrilato (PMMA).
116Tabella 5
Schema base della depolimerizzazione indotta da un processo di degra-
dazione termica [25]
Nel caso di questo polimero si osserva che, una volta avvenuta la rot-
tura iniziale dei legami, la reazione di depropagazione procede lungo la
catena, dando luogo alla formazione di circa 200 unità monomeriche per
unità di scissione iniziale.
Il monomero rappresenta l’unico prodotto finale della degradazione ter-
mica del PMMA che si ottiene con una resa praticamente uguale al 100%
[25].
- Reazioni che coinvolgono i sostituenti laterali
Questo tipo di degradazione si caratterizza per il fatto che
«il polimero conserva la struttura a catena, la cui composizione chimica è
però diversa da quella originale, a causa di reazioni di :
• eliminazione;
• ciclizzazione» [27].
Reazioni di eliminazione causate dal calore, sono state documentate nel
caso del polivinil cloruro (PVC) e del polivinil acetato (PVAC) che, a
temperature relativamente elevate (200 °C per il PVC), eliminano rispet-
tivamente una molecola di HCl e di CH3-COOH per unità ripetitiva
secondo gli schemi della figura 38.
L’eliminazione di acido cloridrico e di acido acetico porta alla forma-
zione di un doppio legame [(prodotto b) in figura 38] che provoca la
destabilizzazione dell’unità ripetitiva adiacente. Il procedere della rea-
zione lungo la catena determina come prodotto finale una macromoleco-
la coniugata dove doppi legami C = C si alternano a legami semplici C–C
[(prodotto c) in figura 38] [25].
117Fig. 37: Le reazioni relative alla degradazione termica (in assenza di ossigeno) del
Polimetilmetacrilato (PMMA) secondo il meccanismo di depolimerizzazione [25].
Queste strutture, caratterizzate da una sequenza di doppi legami coniu-
gati, sono responsabili dell’effetto di scolorimento che si osserva nel
PVC quando subisce questo tipo di degradazione termica [25, 27].
In polimeri, quali l’acido poliacrilico e il poliacrilonitrile, lungo la cui
catena sono presenti rispettivamente gruppi carbonilici (-COOH) e nitri-
lici (-CN), il processo degradativo porta a prodotti con strutture cicliche
(vedasi figura 39) [25, 27].
118Fig. 38: Esempi di degradazione termica con eliminazione dei sostituenti laterali: caso del poli-
vinil cloruro e del polivinil acetato [25].
Fig. 39: Processi di degradazione termica di polimeri attraverso reazioni dei sostituenti laterali
che portano a strutture cicliche: a) il caso dell’acido poliacrilico; b) il caso del poliacrilonitrile
[25 e 27].
119B3 ) Termo – ossidazione e Foto – ossidazione
I polimeri organici e tra questi le macromolecole fibrose (cellulosa,
cheratina e fibroina), costituenti principali delle fibre naturali di interes-
se tessile (lino, cotone, lana, seta, ecc.), reagiscono con l’ossigeno atmo-
sferico anche se la velocità di ossidazione si caratterizza per una cinetica
relativamente lenta.
Al contrario l’ossigeno reagisce velocemente con i radicali, presenti
nella massa polimerica, prodotti dal calore e dalla luce.
A seconda che la fonte primaria dei radicali sia la luce oppure il calore
il processo di ossidazione viene definito rispettivamente di foto-ossida-
zione e di termo-ossidazione.
Questi processi, che dipendono fortemente dalle caratteristiche chimi-
co-strutturali del polimero e dalle condizioni ambientali, possono pro-
durre fenomeni di scissione dei legami covalenti della catena polimerica,
di reticolazione, di emissione di sostanze volatili e di formazione di grup-
pi funzionali contenenti ossigeno.
«L’ossidazione avviene attraverso un meccanismo radicalico a catena che è
sostanzialmente indipendente dal tipo di energia utilizzata per creare i radi-
cali nella reazione di inizio» [22].
Le varie fasi del processo di termo-ossidazione o di foto-ossidazione
sono schematicamente delineate nella figura 40.
Il meccanismo della fase di iniziazione è praticamente uguale a quello
già descritto per la foto-degradazione e termo degradazione in assenza di
ossigeno.
La reazione di propagazione vede il coinvolgimento di macroradicali
polimero * e perossili (polimero – OO*) [(vedasi rispettivamente schema
b1) e b2) in figura 40)] [25, 27].
La reazione che comporta l’estrazione di idrogeno (b2 in figura 40),
essendo più lenta di quella in cui il radicale polimero reagisce con l’ossi-
geno (b1 in figura 40), a parità di ogni altra condizione, di fatto determi-
na la velocità globale della fase di propagazione del processo di termo-
ossidazione o di foto-ossidazione.
Va sottolineato che in strutture fibrose caratterizzate dall’alternanza
lungo l’asse di fibra di regioni cristalline (alta densità e bassa permeabilità
all’ossigeno) e amorfe (bassa densità e alta permeabilità all’ossigeno) si
verifica che il processo di ossidazione avviene preferenzialmente nelle
zone disordinate della fibra laddove la concentrazione dell’ossigeno è
120Fig. 40: Schema globale delle varie fasi, e relative reazioni, dei processi di termo-ossidazione e
di foto-ossidazione [25].
maggiore. Pertanto le regioni di un materiale polimerico a più alta cristal-
linità, in generale, mostrano una maggiore resistenza all’ossidazione.
Le reazioni che caratterizzano la fase di terminazione del processo sono
descritte nella figura 41 [26].
«In condizioni normali di concentrazione di ossigeno, la concentrazione dei
radicali P* (Polimero * in figura 41, n.d.A.) è molto bassa e la reazione di
terminazione avviene per combinazione di radicali POO* (Radicali
Perossili, Polimero – O – O * in fig. 41, n.d.A.) con formazione di un peros-
sido che evolve poi in modo diverso a seconda che i radicali perossile siano
o no terziari … … In difetto di ossigeno anche i radicali P* possono parte-
cipare alla reazione di terminazione [reazione b) in figura 41 n.d.A.]» [27].
121Fig. 41: Le reazioni che caratterizzano la fase di terminazione di un processo di foto-ossidazio-
ne o di termo-ossidazione [26].
La reazione di terminazione c), descritta in figura 41, porta alla retico-
lazione delle catene polimeriche
«Poiché i centri radicalici al carbonio (P*) e all’ossigeno (POO*) che pro-
pagano il processo sono in genere distribuiti lungo la catena polimerica
……. » [27].
Durante il processo di propagazione (vedasi reazioni b) in figura 40) si
formano dei gruppi idroperossidici (Polimero – OO – H) distribuiti lungo
la catena polimerica. In questi gruppi i legami perossidici hanno una bassa
energia (~ 40 K cal / mole) pertanto assorbendo energia termica o fotoni-
ca (da radiazioni elettromagnetiche con lunghezze d’onda anche superio-
ri ai 300 nm) si dissociano facilmente, anche a temperatura ambiente. Da
ciò segue che in condizioni ambientali favorevoli ai processi di foto e
termo – ossidazione i gruppi idroperossidici attraverso una scissione omo-
litica danno luogo alla formazione di radicali Polimero – O * e *OH
(vedasi reazione riportata in figura 42 – a). Questi ultimi hanno la capa-
cità di estrarre atomi di idrogeno dalle catene polimeriche secondo gli
schemi di reazione b) e c) della figura 42 [27].
I radicali alcossilici (Polimero – O *) inducono, anche, reazioni che
122portano alla rottura del legame in al centro radicalico sull’ossigeno con
formazione di un carbonile aldeidico o chetonico.
«Il risultato complessivo della scissione dei gruppi idroperossido è quindi
quello di iniziare nuove catene cinetiche alimentando il processo di propaga-
zione con nuovi radicali…… Con il progredire del processo di ossidazione, la
complessità dei prodotti che si formano aumenta notevolmente con l’ossida-
zione dei gruppi alcolici e carbonilici che porta ad acidi, esteri. ecc.» [27].
Nel caso delle fibre poliammidiche i processi di termo-ossidazione, in
fase solida vengono accelerate dalla presenza di acqua assorbita dalle
regioni amorfe.
Questo fenomeno è da mettere in relazione con il fatto che l’acqua,
agendo da plastificante, abbassa la Tg; conseguentemente la mobilità dei
segmenti macromolecolari aumenta e quindi il materiale diviene più
facilmente accessibile alle molecole di ossigeno.
«Gli effetti chimici principali dell’ossidazione sono l’aumento dei gruppi
carbossilici e la contemporanea diminuzione di quelli amminici; anche la
massa molecolare diminuisce. La degradazione termoossidativa procede
mediante reazione a catena di radicali liberi che coinvolgono l’atomo di C in
al gruppo -CONH- con formazione di idroperossido e rigenerazione di un
alchil radicale, che a sua volta reagisce ancora con ossigeno per dare un radi-
cale perossidico e così via» [29].
Fig. 42: Reazioni di propagazione, relative al processo secondario di foto-ossidazione e termo-ossi-
dazione, indotte dalla scissione dei gruppi idroperossido formatisi durante la fase iniziale [25, 27].
123Fig. 43: Le varie fasi che portano alla termo-ossidazione delle poliammidi. Il radicale R*, forma-
tosi per azione della luce, calore, impurezze, ecc., reagisce sul -CH2- prossimo al gruppo -NH- [29].
Le varie fasi che, partendo dal radicale R * formatosi per effetto del-
l’incidenza di radiazioni luminose, del calore, impurezze o additivi, por-
tano alla decomposizione delle poliammidi in ammide ed aldeide, sono
delineate nella figura 43 [29].
«Le reazioni che conducono alla decomposizione di (VI) in ammide ed
aldeide sono in accordo, sia con la diminuzione delle masse molecolari che
accompagna la termoossidazione e le fotoossidazioni, sia con l’assorbimen-
to mediante spettrometria del gruppo >C=C< aldeidico. Invece la diminu-
124zione di gruppi amminici probabilmente può aver la seguente origine: l’ul-
teriore ossidazione del componente aldeidico porta a formare il gruppo
–COOH, che condensa con i gruppi amminici presenti» [29].
Durante il processo di termo-ossidazione delle poliammidi si osserva
un fenomeno di ingiallimento il quale sembra che debba essere ascritto
alla formazione di gruppi cromofori originatesi
«sia da autocondensazioni aldeidiche, sia da condensazioni tra gruppi ammi-
nici ed aldeidici. Tuttavia è da osservare che le sostanze cromofore possono
formarsi anche per ulteriori ossidazioni e ciclizzazioni in prodotti di reazio-
ne aldeidici» [29]
La fotodegradazione delle poliammidi allo stato fibroso, determinata dal-
l’esposizione alla luce solare anche a temperatura ambiente, comporta:
- la riduzione delle masse molecolari;
- il decremento dello sforzo massimo a trazione;
- la diminuzione dell’allungamento a rottura.
Il processo di fotolisi che conduce alla rottura del legame C-N, che nel
caso delle poliammidi alifatiche è il legame cui corrisponde una minore
Fig. 44: Le possibili reazioni che si verificano durante il processo di fotodegradazione e in par-
ticolare della fotolisi delle poliammidi alifatiche [29].
125energia, è da mettere in relazione con l’assorbimento da parte del gruppo
ammidico -NH-CO- di quanti fotonici aventi lunghezza d’onda inferiore
a 300 nm.
Le reazioni connesse al processo di fotolisi delle poliammidi alifatiche
sono illustrate nella figura 44, dalla quale si evince che i radicali forma-
tisi a seguito della
«scissione del legame ammidico estraggono un atomo di idrogeno da -CH2-
in posizione vicinale () a -NH- ; il gruppo metilenico costituisce la princi-
pale fonte di radicali liberi…..» [29].
Per quanto riguarda la foto-ossidazione delle poliammidi è stato dimo-
strato che gli stadi iniziali ed i prodotti derivati sono praticamente gli
stessi della termo-ossidazione. Inoltre, è stato osservato che la velocità di
foto-ossidazione praticamente corrisponde alla velocità di formazione
dell’idroperossido (vedasi figura 43).
«A temperatura ambiente la formazione (dell’idroperossido) richiede oltre
100 ore. Come previsto, lunghezze d’onda più brevi (Fig. 45: Struttura chimica degli amminoacidi tirosina e triptofano i cui residui sono presenti nelle
catene proteiche delle fibre di lana.
che conducono a prodotti di degradazione di natura diversa [26].
A titolo esemplificativo alcune delle possibili reazioni che determinano
il deterioramento delle fibre tessili indotte da radicali ossi-fibra sono
riportate nella figura 46. In particolare i processi in a) e in b) portano alla
rottura della catena macromolecolare con la formazione rispettivamente
di un gruppo chetonico e di un gruppo aldeidico terminale [26].
«If the deterioration products contain a chromophoric group, such as a
ketone or aldehyde group, which can be part of a chromophoric system, the
colour of the fibre will change. If covalent bonds in the polymer chain back-
bone undergo rupture (causing chain scission) a decrease in DP (grado di
polimerizzazione; n.d.A.) occurs, and thus a change in the mechanical prop-
erties of the fibre, which is manifested in the decrease of its mechanical
strength» [26].
127La foto-ossidazione «is an autocatalytic chain reaction process» che, relativa-
mente alla prima fase, dipende fortemente dai seguenti fattori:
- lunghezza d’onda, energia ed intensità della luce;
- durata dell’esposizione alla luce.
È stato provato sperimentalmente che, in generale, la presenza nelle
fibre tessili di particelle di polvere con spigoli molto aguzzi, di enzimi, di
microrganismi e tracce di catalizzatori, insieme ad un elevato contenuto
di acqua, provocano un sensibile aumento della velocità delle reazioni di
fotodeterioramento e questo sia nella fase primaria che secondaria.
Secondo quanto riportato da A. Tímár-Balazsy e D. Eastop il processo
di foto-ossidazione si caratterizza per un primo stadio relativamente lento
(fase di induzione), successivamente la velocità aumenta, raggiunge un
valore massimo e quindi, man mano che i siti accessibili all’ossigeno
lungo le macromolecole si esauriscono, diminuisce.
Il meccanismo sopra esposto spiega il perché in alcune circostanze e a
basse temperature il fenomeno di scolorimento non necessariamente si
osserva durante l’esposizione dell’oggetto (ad esempio un tessuto) alla
luce ultravioletta ma solo in un secondo momento [26].
Dall’analisi della letteratura è possibile trarre le seguenti conclusioni, di
carattere generale, che riguardano la foto-degradazione / foto-ossidazio-
ne delle fibre tessili.
Fig. 46: Possibili reazioni che, partendo da radicali – ossi – fibra, portano alla scissione delle
macromolecole elementari componenti una fibra naturale [26].
128a) I processi di foto-degradazione / foto-ossidazione ed i relativi
effetti di deterioramento sulle fibre non avvengono nel vuoto, ciò
significa che l’ossigeno atmosferico e l’umidità giocano un ruolo
attivo e fondamentale.
b) Particolarmente efficaci ai fini della foto-degradazione sono le
radiazioni ultraviolette, essendo caratterizzate da un’energia suf-
ficiente a provocare la rottura di legami interatomici covalenti.
c) La durata dell’esposizione è un fattore di grande rilevanza poi-
ché l’effetto è di natura cumulativo.
d) Il calore dell’ambiente facilita fortemente i processi di foto-dete-
rioramento.
Da quanto sopra si ricava che i manufatti tessili possono essere esposti
alla luce per periodi di tempo relativamente brevi, solo se da questa sono
state filtrate le radiazioni della banda ultravioletta. Comunque l’intensità
della luce necessaria alla loro fruibilità deve essere ridotta al minimo.
Inoltre bisogna assolutamente evitare che nei locali, a basso grado di
umidità, siano presenti lampade capaci di generare calore (ad esempio
quelle ad incandescenza). Il fatto che le fibre tessili, siano esse di origine
naturale che di natura sintetica, siano particolarmente sensibili all’azione
degradativa della luce solare viene documentato, a titolo esemplificativo,
dalle due micrografie messe a confronto nella figura 47. In particolare
nella figura 47 – a sono mostrate le fibre di polipropilene non stabilizza-
te e non ancora sottoposte all’azione delle radiazioni solari; le fibre
appaiono integre con la superficie liscia che non mostra segni di deterio-
ramento. Al contrario fibre di polipropilene, non stabilizzate, esposti alle
radiazioni solari denotano evidenti fenomeni di degradazione che si
manifestano attraverso profonde fratture e buchi presenti lungo tutta la
loro lunghezza (vedasi figura 47 – b) (30).
Da quest’esempio emerge chiaramente quanto grave, profondo e desta-
bilizzante possa essere un attacco degradativo indotto dall’azione combi-
nata della luce e dell’ossigeno (foto – ossidazione) oppure della luce e del
calore (termo – ossidazione).
129a)
b)
Fig. 47: Micrografie elettroniche di: a) fibre di polipropilene integre; b) fibre di polipropilene
non stabilizzate degradate per effetto della esposizione alla luce solare [30].
130B4 ) Foto-ossidazione e Termo-ossidazione delle fibre naturali
B4,1 ) Foto-ossidazione delle fibre di lana
Le fibre di lana sottoposte all’azione di radiazioni UV ( < 380 nm)
subiscono un processo di foto – ossidazione che da luogo a fenomeni di
deterioramento foto-chimico i cui sintomi sono rappresentati da un
ingiallimento e decadimento delle caratteristiche meccaniche (ad esem-
pio infragilimento). La presenza di umidità aumenta fortemente la sensi-
bilità della lana alla foto-ossidazione. Infatti la velocità di ingiallimento,
misurata in condizioni di elevata umidità, è all’incirca dieci volte mag-
giore di quella determinata in un ambiente secco [26].
La luce visibile, in particolare le radiazioni con comprese tra 380 –475
nm, può, a sua volta, causare lo sbiancamento di fibre di lana ingiallite.
G. C. Ramsay riportava, in un suo interessante articolo del 1970 [31],
che i residui di aminoacidi, presenti lungo la catena proteinica dell’
cheratina, più sensibili all’assorbimento di radiazioni del vicino ultravio-
letto erano quelli dell’istidina, del triptofano, della tirosina, della metio-
nina, della cistina e della cisteina. Inoltre, lo stesso Autore metteva in
risalto come, nel caso della lana, le reazioni foto-chimiche, indotte da
radicali liberi, potessero portare a nuove reticolazioni, alla rottura di reti-
colazioni preesistenti e alla rottura di legami peptidici (vedasi figura 48).
L’insieme di questi processi sono causa di profonde variazioni di natura
chimica, fisica e comportamentali (ad esempio il decadimento delle
caratteristiche meccaniche delle fibre) [31, 26, 32].
Le reazioni chimiche che portano alla formazione di nuove reticolazio-
ni sono provocate da radicali ossidrili originatisi a seguito di processi
fotochimici primari.
Il radicale *OH può reagire con due gruppi tiolo (SH), presenti nei resi-
dui della cisteina, appartenenti a due catene proteiche diverse oppure alla
stessa macromolecola. Nel primo caso (figura 49-b) si forma un legame
disolfuro (– S – S –) di natura inter-molecolare, nel secondo di natura
intra-molecolare (figura 49-c) [26].
L’assorbimento di radiazioni con < 310 nm provoca una reazione di
foto-ossidazione primaria che porta alla rottura di legami disolfuro a cui
fa seguito la formazione di gruppi solfonici (sensibili all’acqua) (figura
50) [26, 31].
In ambiente con alti valori dell’umidità relativa i gruppi solfonici faci-
131Fig. 48: Rappresentazione schematica delle modifiche indotte da reazioni fotochimiche in fibre di
lana esposte all’azione di radiazioni appartenenti al vicino ultravioletto: 1) scissione delle catene
proteiche; 2) formazione di nuove reticolazioni; 3) distruzione di reticolazioni preesistenti [32].
litano una reazione di idrolisi acida dei legami peptidici presenti lungo la
macromolecola dell’cheratina. Il residuo della cistina, quando è lega-
to al residuo della tirosina (figura 51-a), è sensibile all’attacco degradati-
vo dei radicali liberi. Infatti la tirosina ha la capacità di assorbire radia-
zioni UV attivando una reazione di fotolisi che conduce alla formazione
di zolfo-radicali (*S-) (figura 51-b) che, reagendo con molecole di acqua,
formano gruppi laterali –SH e –SOH (figura 51-c). Sempre in presenza di
acqua i gruppi –SOH si trasformano in gruppi aldeidici con sviluppo di
idrogeno solforato (figura 51-d) [26].
Il processo di foto-ossidazione delle fibre di lana, indotto dall’assorbi-
mento di radiazioni UV, comporta la rottura di cross link disolfuro, di
legami peptidici, di legami ionici e di natura secondaria. Questi fenome-
ni causano, tra l’altro, un aumento della solubilità delle catene di che-
ratina che risultano più accessibili all’azione di acidi ed alcali. Dal punto
di vista meccanico le fibre di lana foto-deteriorate mostrano una sensibi-
le riduzione dell’allungamento a rottura [26].
A.Tímár – Balázsy e D. Eastop hanno messo in evidenza che durante il
corso del processo di foto-ossidazione la rottura delle catene polipeptidi-
che e la formazione di reticolazioni tra catene diverse può avvenire attra-
132a)
b)
c)
Fig. 49: Foto-ossidazione delle fibre di lana. Formazione di nuove reticolazioni disol-
furo (-S-S-): a) un radicale ossidrile reagisce con due gruppi tiolo cisteinici apparte-
nenti a due macromolecole adiacenti; b) formazione di un legame disolfuro inter-cate-
na; c) il radicale ossidrile reagendo con due gruppi tiolo della stessa catena forma un
legame disolfuro intra-catena [26].
verso la formazione di cross link che coinvolgono gruppi disolfuro, pep-
tidici ed i residui degli aminoacidi lantionina e lisinoalanina.
A seguito di queste trasformazioni le fibre di lana acquisiscono una
struttura con un maggiore grado di reticolazione, pertanto esse saranno
caratterizzate da una maggiore rigidità e quindi fragilità a cui si accom-
pagna una minore flessibilità ed una minore attitudine ad assorbire acqua
dall’ambiente [26].
Secondo D. J. Carlsson e D. M. Wiles la causa principale dell’ingialli-
mento osservato quando le fibre di lana sono esposte all’azione della luce
solare è principalmente dovuto alla foto-ossidazione dei residui del trip-
tofano che reagiscono con l’ossigeno, in uno stato di singoletto, genera-
to dalla foto-eccitazione dei gruppi della tirosina (vedasi schema delle
reazioni in figura 52-a) [33].
133Fig. 50: Foto-ossidazione della lana: rottura di cross link disolfuro (-S-S-), causata da reazioni di
foto-ossidazione primaria indotte dall’assorbimento di luce (lunghezza d’onda < 310 nm) che
porta alla formazione di gruppi solfonici acidi laterali [26].
La produzione di zolfo-radicali viene spiegata ammettendo che duran-
te il processo si verifichi anche la foto-rottura dei ponti zolfo della cisti-
na. Tra l’altro viene anche osservata la rottura dei residui degli ammi-
noacidi glicina ed alanina, presenti lungo lo scheletro molecolare. I mec-
canismi foto-chimici relativi a queste ultime reazioni sono mostrati in
figura 52–b [33].
J. S. Crighton in relazione al fenomeno di ingiallimento della lana ha
scritto:
134Fig. 51: Rottura di cross link disolfuro (-S-S-) e formazione di gruppi laterali cisteinici e di natu-
ra aldeidica [26].
«The yellowing of the wool by the transformatin of the tryptophan residue
to a chromophore has been examined by several workers. Tyrosine and his-
tidine residues have also both been implicated in the photo-yellowing of
wool. Dyes can also sensitise the photodegradation of wool» [34].
Il meccanismo attraverso il quale i coloranti possono partecipare e sen-
sibilizzare i processi di foto-degradazione delle fibre di lana è descritto
schematicamente nella figura 53.
Il triptofano, la tirosina e l’istidina rappresentano i residui di amminoa-
cidi, presenti lungo la catena dell’cheratina, che più degli altri posso-
no partecipare al tipo di processo descritto nella figura 53, reso possibile
dalla presenza attiva di molecole di coloranti. Sembra che il tutto preve-
da l’assorbimento di ossigeno e l’emissione di anidride carbonica [34].
La sensibilità spettrale delle fibre di lana, definita dall’intervallo di lun-
ghezza d’onda delle radiazioni incidenti in corrispondenza del quale si
135a)
b)
Fig. 52: Foto-ossidazione della lana: a) le possibili reazioni che provocano il fenomeno di ingial-
limento delle fibre (vedasi testo); b) reazioni collaterali che portano alla rottura dei residui della
glicina e dell’alanina [33].
Fig. 53: Foto-ossidazione della lana: caso in cui i coloranti possono sensibilizzare il processo
fotodegradativo. In figura viene descritto lo schema delle reazioni [34].
136Fig. 54: Foto-ossidazione della lana: Diagramma a barre attraverso il quale è possibile eviden-
ziare le lunghezze d’onda dello spettro solare in corrispondenza del quale si verifica il maggiore
danno (sensibilità spettrale). La sensibilità spettrale della lana viene confrontata con quella di
altri polimeri. La colonna a destra riporta la metodologia seguita per quantificare il grado di dete-
rioramento indotto [35, 36].
osserva il maggiore grado di foto-deterioramento, è confrontata con quella
di altri polimeri e materiali nel diagramma a barre della figura 54 [35, 36].
In particolare, nel caso della lana è stato assunto, come sintomo del
danno arrecato il grado di ingiallimento; per altri materiali il fattore pre-
scelto indicativo del degrado è di natura diversa (ad esempio, densità otti-
ca, grado di depolimerizzazione e di rottura delle catene, estensibilità,
ecc.). Come si evince dalla figura 54, la lana mostra un massimo valore
dell’indice di ingiallimento per lunghezze d’onda della luce incidente
comprese tra 290 e 311 nm. Nel caso di esperimenti condotti con luce
monocromatica la lunghezza d’onda della luce che provoca il maggior
danno è quella che ha una pari a 280 nm [35, 36].
Abrasioni e rotture, tipiche di un processo di foto-ossidazione, dovuta
all’esposizione della luce solare, rilevate mediante microscopia elettroni-
ca su di un campione di fibre di lana prelevate da un tappeto Holbein del
XVI secolo (Ushak-Anatolia) sono evidenziate nella micrografia riporta-
ta nella figura 55 [13].
L’esposizione delle fibre di lana alla luce solare, come già precedente-
mente scritto, provoca sensibili variazioni di natura fisica e chimica le
quali si evidenziano, a livello macroscopico, attraverso un fenomeno di
ingiallimento (discolouration) collegato alla formazione di prodotti di
foto-degradazione di colore giallo. Per tempi prolungati di esposizione, si
137Fig. 55: Foto-ossidazione della lana: Micrografia elettronica di un campione di fibre di lana pre-
levate da un tappeto Holbein del secolo sedicesimo. Sono evidenti rotture tipiche di un processo
di foto-degradazione [13].
osserva una riduzione della resistenza a trazione e della resistenza all’a-
brasione (phototendering) ed una alterata attitudine alla tintura [37].
Confrontando lo spettro di assorbimento UV della cheratina di lana
Merino con quello calcolato sulla base della composizione amminoacidi-
ca (vedasi figura 56), si ricava che, per lunghezze d’onda superiori a 290
nm la lana presenta un potere assorbente maggiore di quanto ci si aspet-
terebbe da un punto di vista teorico. R. S. Davidson in relazione a questo
comportamento scrive:
«In the region above 290 nm, the wool fibre is more strongly absorbing than
expected, and it is concluded that absorption in this region may be due to the
presence of natural pigment precursors» [37].
Come si evince dall’andamento delle curve riportate nella figura 57 il
grado di ingiallimento delle fibre di lana è funzione della percentuale di
acqua assorbita e della natura dei trattamenti, anche di natura chimica (ad
esempio il “bleaching” o candeggio), eventualmente subiti.
138Fig. 56: Spettro di assorbimento UV, sperimentale (sezione radicale di lana Merino, curva con-
tinua) e teorico (calcolato sulla base della composizione amminoacidica, curva tratteggiata). La
curva a linee e punti rappresenta l’intensità relativa della luce solare nella città di Sidney alle ore
12 a.m. [37].
E’ interessante sottolineare il fatto che quando le fibre di lana sono sot-
toposte all’azione della luce solare i processi di ingiallimento e di imbian-
chimento partono contemporaneamente. Quello che si osserverà dipen-
derà dall’intensità relativa delle varie lunghezze d’onda incidenti e anche
dal grado di ingiallimento iniziale della lana [37].
Come già precedentemente scritto la fotodegradabilità della lana trova
la sua causa nella intrinseca fotolabilità dei residui di amminoacidi costi-
tuenti e dalla presenza di prodotti e pigmenti derivanti da reazioni di altra
natura (non fotochimiche).
In generale nel caso di proteine fibrose, i residui di -amminoacidi più
sensibili alla degradazione fotochimica sono quelli del triptofano, dell’i-
stidina, della cisteina e della cistina, le cui strutture chimiche sono illu-
strate nella figura 58.
R. S. Davidson riporta che l’ingiallimento della lana con radiazioni sola-
139a) b)
Fig. 57: Influenza dell’acqua sul processo di foto-ingiallimento delle fibre di lana in funzione
anche del trattamento subito (whitened o bleached): a) fibre secche (dry); b) fibre umide (wet)
[37].
a) b)
Fig. 58: Struttura molecolare degli -amminoacidi, i cui residui sono presenti nelle macromole-
cole proteiche della lana e di altre proteine fibrose, più sensibili alla degradazione fotochimica:
a) Triptofano; b) Istidina.
140Fig. 58:
c)
c) Cistina e cisteina.
ri genera molecole di ossigeno che si trovano nello stato di singoletto (1O2).
Questa osservazione porta all’ipotesi che la degradazione del triptofano e
della cistina siano in gran parte attribuiti ad ossidazioni conseguenti a rea-
zioni con molecole di 1O2. I prodotti della fotodegradazione del triptofano,
via ossidazione con 1O2, sono mostrati nella figura 59 [37].
L’ossidazione della cistina via 1O2, comporta la formazione iniziale di un
monossido-derivato e, successivamente, di un diosside. Quindi, in presen-
za di acqua si osserva la rottura del legame S–S con l’ottenimento di acido
cisteico ed un residuo cisteinico (vedasi schema in figura 60) [37].
La presenza di idroperossidi rappresenta una fonte di radicali derivanti
dalla rottura omolitica del legame RO—OH a seguito di esposizione alla
luce. Le specie radicali che si formano (RO * e HO *) e in particolare
quelle di natura ossidrilica (HO *), come si evince dagli schemi di rea-
zione riportati nella figura 61, possono dare luogo ad una vasta gamma di
percorsi degradativi delle fibre di lana.
«This radical is a powerful hydrogen abstracting species, which is perfectly
capable of abstracting hydrogen from the -C-H bond of amino acids, the
N-H bond of tryptophan and imidazole and the S-H bond of cystine. It is also
capable of generating phenoxyl radicals from phenols and of the hydroxyla-
tion of aromatic residues such as those found in tyrosine, phenylalanine and
141tryptophan. With products such as derivatives of ketocarboxylic acids being
formed, there is the possibility of chain cleavage, since such compounds are
highly susceptible to photo-oxidation break-down. Similarly, the formation
of hydroxylated tryptophan and quinols leads to the possibility of the pro-
duction of quinines and related species, which can undergo further conden-
sation reactions leading to the final product melanin» [37] (figura 61).
Dal lavoro di R. S. Davidson è stato possibile trarre le seguenti rilevanti
conclusioni.
Fig. 59: Prodotti derivati dalla fotodegradazione del triptofano via ossigeno singoletto [37].
Fig. 60: Foto-degradazione della cistina via ossigeno singoletto [37].
142I. Le radiazioni UV ( < 350 nm) provocano la rottura del legame
– S – S – della cistina e degradano i residui degli -amminoaci-
di triptofano e tirosina.
II. I processi chimici che comportano la diminuzione del contenuto
di cistina nelle fibre di lana producono di fatto un aumento della
loro fotolabilità.
III. La degradazione dei residui del triptofano, presenti lungo le cate-
ne delle proteine della lana, porta alla formazione di una serie di
prodotti, alcuni fluorescenti, altri fosforescenti, non sempre iden-
tificabili, che assorbono luce nell’intervallo di lunghezza d’onda
che va da 350 a 500 nm, questi prodotti vengono distrutti a segui-
to di irraggiamento con luce la cui è tale da verificare la con-
dizione 380 nm ≤ ≤ 500 nm.
IV. I residui della tirosina a seguito di reazione di fotodegradazione
formano prodotti a struttura sconosciuta, non fluorescente, che
assorbono luce con compresa tra 350 – 500 nm.
V. Al fine di prevenire la formazione di specie molecolari colorate
è necessario distruggere mediante irraggiamento i residui del
triptofano e della tirosina (foto-labile) sottoponendo la lana all’a-
zione della luce in presenza di agenti riducenti [37].
Fig. 61: a) Possibili percorsi fotodegradativi delle fibre di lana, via radicali ossidrilici HO * [37].
143144
Fig. 61: b) Possibili percorsi fotodegradativi delle fibre di lana, via radicali ossidrilici HO * [37].Gli eventi di natura fotofisica e fotochimica che si verificano nella fase
inziale del processo di fotodegradazione della lana, indotto dall’esposi-
zione alle radiazioni UV ( < 310 nm), sono:
a) formazione di cromofori che assorbono radiazioni con < 310 nm;
b) formazione di stati elettronici eccitati dei residui di triptofano;
c) fotodegradazione dei residui del triptofano;
d) fotodegradazione dei residui della tirosina e della cistina;
e) formazione di radicali liberi [38, 39].
Processi di assorbimento di radiazioni aventi ≥ 320 nm devono esse-
re attribuiti a specie chimiche diverse dai residui del triptofano e della
cistina. Queste sostanze cromofore, attive dal punto di vista fotochimico
e, pertanto, capaci di indurre importanti effetti di fotodeterioramento,
possono avere origine da una serie di eventi i più importanti dei quali
sono qui di seguito descritti.
a) Sostanze cromofore derivate da residui di amminoacidi
non aromatici.
E’ stato dimostrato sperimentalmente che, sottoponendo la lana e la seta
all’azione di radiazioni con ≥ 320 nm si osserva la produzione di -
chetoacidi. Questi composti possono derivare da una reazione di trasferi-
mento di un protone tra due gruppi peptidici legati mediante un legame
ad idrogeno appartenenti a due specie radicaliche di -chetoacidi (veda-
si figura 62) [39].
Il fenomeno di ingiallimento superficiale della lana viene spiegato
ammettendo che questi -chetoacidi possono dare luogo, per condensa-
zione aldolica, a prodotti polimerici di colore giallo [39].
b) Cromofori derivati dal triptofano.
Sempre nel riferimento [39] viene riportato che gli -chetoacidi hanno
la capacità di reagire facilmente con i residui del triptofano producendo
dei -carbolinici secondo lo schema delineato nella figura 63. Queste
ultime sostanze assorbono radiazioni UV emettendo per fluorescenza
luce la cui lunghezza d’onda va dal verde al giallo. La struttura chimica
di acidi 1,3 – di carbossilici e di acidi - - carbolinici, estratti da fibre di
lana sottoposte ad irraggiamento, è illustrata nella figura 64.
145Fig. 62: Schema di reazione tra due radicali di chetoacidi che, attraverso il trasferimento di un
protone tra due gruppi peptidici legati da un legame ad idrogeno, porta alla formazione di che-
toacidi [39].
Fig. 63: Schema della reazione tra il triptofano e chetoacidi che porta alla formazione di pro-
dotti fluorescenti (carbolinici) [39].
c) Cromofori derivati dalla tirosina.
Nei riferimenti 40 e 41 è documentata la presenza, in fibre di lana espo-
ste all’azione di radiazioni UV, di di- e tri- tirosina. Questi prodotti, fluo-
rescenti, derivanti da reazioni di ossidazioni del residuo della tirosina,
potrebbero essere l’origine di derivati melaninici, in particolare
l’Eumelanina, trovata all’estremità di fibre di lana da velli di pecora di
colore nero [42,43].
d) Cromofori di natura esogena.
Derivano dalla presenza, nella lana lavata, scoured, di ioni metallici
(ferro e rame) fortemente legati alla lana ed, eventualmente, introdotti
durante le fasi di lavaggio. Questi ioni formano dei veri e propri com-
plessi con le molecole proteiche costituenti la lana, in particolare la che-
ratina, i quali hanno la proprietà di assorbire la luce anche nelle regioni
del visibile. Inoltre questi cromofori, come già scritto precedentemente,
146Fig. 64: Struttura molecolare di acidi 1,3–di carbossilici e di acidi--carbolinici, derivanti da rea-
zioni del tipo di quelle mostrate in fig. 63, estratti da cheratina di fibre di lana sottoposte all’a-
zione degradativa di radiazioni UV (> 320 nm) [39].
hanno la funzione di «sensitize the photodegradation of wool» [39].
Nel caso di processi di lavaggio inadeguati si notano nelle fibre tracce
di cromofori prodotti dalla degradazione della porfirina (ad es. la cloro-
filla). Questi cromofori sono soggetti a fenomeni di foto-imbiancamen-
to. Fibre colorate in colore pastello normalmente cambiano di colore
rapidamente se esposte alla luce. Questo fenomeno è stato attribuito alla
presenza di clorofilla, quale contaminante, la quale sensibilizza il dete-
rioramento del colore [44].
e) Reazioni di ossidazioni fotosensibilizzate
Secondo quanto riportato da G. J. Smith, nel suo già citato lavoro [39],
queste reazioni possono essere divise in due categorie.
Reazioni di tipo-I):
la sostanza fotosensibilizzata reagisce, prima con il substrato formando
un radicale. Successivamente avviene la reazione tra questo radicale e
l’ossigeno.
147Reazioni di tipo-II):
Il fotosensibilizzante, in uno stato eccitato, dà luogo, attraverso una rea-
zione di trasferimento di energia con una molecola di ossigeno che si
trova nel suo stato fondamentale, alla formazione di ossigeno eccitato in
uno stato di singoletto (1O2) che a sua volta reagisce con il substrato.
Le possibili reazioni tra l’ossigeno singoletto ed i residui del triptofano e del-
l’istidina sono descritte nella figura 65 [riferimenti, 124, 128, 118 in rif. 39].
Da tutto quanto sopra riportato emerge quanto sia elevata la comples-
sità dei processi di foto-degradazione della lana.
In relazione a questo aspetto G. J. Smith ha scritto:
«Photodamage to structural proteins is a widespread phenomenon leading to
problems such as the degradation of wool. Because the photodegradation of
wool keratin represents a commercial problem for the wool industry, there
has been a considerable research effort in this area.
In view of the chemical complexity and variability of structural proteins it is
not surprising that their photochemistry is also complex. Although much
attention has focused on tryptophan as a primary chromophore in the pho-
todegragative process it is clear there are many other species which absorb
radiation in the UVB region of the spectrum and at longer wavelengths
which also results in protein degradation» [39].
J. Csapò et Al., hanno determinato la composizione amminoacidica di
fibre di lana prelevate da una serie di tappeti e tessuti vari, di interesse
storico culturale, con l’obiettivo di correlare la percentuale residua di
cistina, acido cisteico, metionina e tirosina con l’età dei manufatti [45].
La metodica è basata sui seguenti presupposti:
i) i due amminoacidi contenenti zolfo (cistina e acido cisteico)
sono molto sensibili a fenomeni di ossidazione, inoltre, in fun-
zione delle condizioni ambientali la cistina può decomporsi in
alanina, omo-cistina e glicina, oppure può trasformarsi in cistei-
na, omo-cistina e glicina;
ii) la metionina per ossidazione si trasforma in metionina-solfone e
solfosside.
In relazione a quanto sopra la metodica è stata sviluppata determinando
la concentrazione degli amminoacidi contenenti zolfo nello stato ossidato.
I campioni di fibre di lana analizzati sono stati prelevati, in parte da tap-
peti di origine copta conservati presso “l’Hungarian Applied Arts Museum”,
148Puoi anche leggere