ORTHOMYXOVIRUS AA 2019-2020 - GIOVANNI DI BONAVENTURA, PHD UNIVERSITÀ DI CHIETI-PESCARA CDS MEDICINA E CHIRURGIA - SCUOLA DI MEDICINA E SCIENZE ...
←
→
Trascrizione del contenuto della pagina
Se il tuo browser non visualizza correttamente la pagina, ti preghiamo di leggere il contenuto della pagina quaggiù
Orthomyxovirus
Giovanni Di Bonaventura, PhD
Università di Chieti-Pescara
CdS Medicina e Chirurgia
AA 2019-2020Orthomyxovirus
Caratteri generali
▪ Famiglia Orthomyxoviridae, comprendente 5 generi (o tipi):
▪ Virus influenzali A, B, C patogeni per l’uomo (A anche per suini, uccelli)
▪ Thogotovirus, modesta patogenicità per l’uomo
▪ Isavirus, patogeno nei pesci
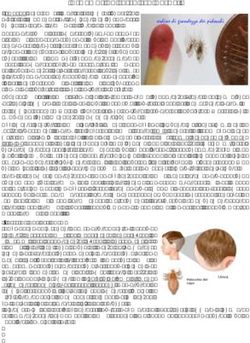
▪ Virione (d=80-120 nm) pleomorfo (sferici o filamentosi)
▪ Envelope dotato di proiezioni formate da glicoproteine
(emoagglutinina, HA; neuraminidasi, NA; HA/NA=5)
▪ Matrice costituito da proteina M, precursore delle proteine
M1 ed M2 che intervengono nella fase di maturazione
▪ Nucleocapside (d=9-15 nm) a simmetria elicoidale,
contenente:
▪ genoma (12-16 kb) costituito da ssRNA segmentato (8 segmenti in A e B; 7 in C per assenza di NA,
sebbene la sua funzione sia vicariata da HA); ogni segmento (senso -) è associato ad una
nucleoproteina (NP)
▪ trascrittasi (RNA-pol-RNA-dipendente) (subunità PB1, PB2, PA)
▪ NS1, NS2: regolano trasporto RNA genomico, evitandone lo splicing; NS1 regola morfogenesi viraleOrthomyxovirus
Emoagglutinina e neuraminidasi
▪ Emoagglutinina (H) = trimero con forma di spicola, è l’antirecettore H
▪ riconosce residui di acido sialico legato a Gal mediante legame
α-2,6 (adsorbimento)
▪ ciascuna subunità viene attivata da una proteasi che la scinde in
2 porzioni unite da legami S-S
▪ proteina di fusione (scapsidazione)
▪ stimola la produzione di anticorpi neutralizzanti
▪ agglutina gli eritrociti umani
▪ modificazioni nella sua struttura (18 tipi: HA1-H18; solo HA1,
HA2 e HA3 stabili nell’uomo) causano variabilità antigenica
minore (“drift” o deriva antigenica) e maggiore (“shift”)
N
▪ Neuraminidasi (N) = tetramero dotato di attività enzimatica
▪ taglia il residuo di acido sialico delle glicoproteine (recettore
cellulare), prevenendo l’agglutinazione dei virioni e
facilitandone la liberazione
▪ subisce modificazioni soltanto nel virus influenzale tipo A (11
tipi: N1-N11; solo N1 e N2 stabili nell’uomo)Orthomyxovirus
Ciclo replicativo
1. Adsorbimento virale, mediato da HA (HA1-18, tropismo), a
residui di acido sialico di glicoproteine di superficie cellulare
ed internalizzazione per endocitosi mediata da recettore
2. Scapsidazione: acidificazione endosomale (per opera di M2 che agisce da pompa
protonica), modificazione HA2 e attivazione proteolitica con fusione envelope-
membrana endocitica HA-mediata; liberazione del nucleocapside e degradazione
capside. Migrazione complessi RNP verso il nucleo* (NP-mediata)
3. Trascrizione genoma (RNA-pol-RNA-dip virale) e formazione di cap-mRNA-poliA
◼ frammenti RNA cellulare necessari per «innesco» trascrizione
4. Traduzione citosolica mRNA in proteine (NS1-2, PB1-2, NP, M1-2)
4. Modificazione (glicosilazione) HA e NA nel RE e nel Golgi e trasferimento verso membrana
5. Replicazione del genoma in sede nucleare
▪ protezione di RNA genomico da splicing
6. Trasferimento RNA genomico nel citosol, associazione con NP e assemblaggio di nucleocapsidi
7. Gemmazione apicale mediata da proteina M1 e liberazione virioni facilitata dal clivaggio dei residui
di acido sialico da parte di NA
*eccezione in RNA-virusOrthomyxovirus
Nomenclatura
▪ Nomenclatura ceppi tipo A
▪ tipo
▪ luogo primo isolamento
▪ numero sequenziale isolamento
A/Moscow/10/1999(H3N2)
▪ anno del primo isolamento
▪ sotto-tipo (assetto antigenico NA e HA)
▪ Nomenclatura ceppi tipo B
▪ tipo
▪ luogo primo isolamento
B/Hong Kong/330/2001
▪ numero sequenziale isolamento
▪ anno del primo isolamento
Un solo sierotipo: tasso di mutazione 2-3 vv inferiore vs. tipo A; minore diversità geneticaOrthomyxovirus L’assetto M1, M2, NP determina
la distinzione nei 3 sierotipi
Variabilità genica
Tipo A: reservoir animale (uccelli acquatici); anatra (asintomatica, ad eccezione di virus con H5 o H7
che causano epizoozie ad elevata mortalità) infetta suino/pollo che, a sua volta, infetta l’uomo;
possibili epidemie e pandemie
Tipo B: circolazione interumana; può causare epidemie
▪ La presenza di un genoma segmentato conferisce ai virus influenzali una
rilevante variabilità genetica:
▪ mutazione geni per H ed N
▪ antigenic “drift” (modificazioni antigeniche minori) nei virus A e B
▪ 18 sottotipi H e 11 sottotipi di N, presenti in differenti combinazioni
▪ fenomeni epidemici (a cadenza quasi annuale)
▪ riassortimento tra genomi di ceppi diversi
▪ antigenic “shift” (modificazioni antigeniche maggiori) solo in tipo A
▪ epitelio respiratorio del suino viene co-infettato da virus aviario e virus
umano, in quanto presenta residui di acido sialico legato a galattosio
sia mediante legame α-2,3 (virus umano) che α-2,6 (virus aviario)
▪ fenomeni pandemici (H1N1: «spagnola», 1918; H2N2: «asiatica»,
1957; H3N2: «Hong Kong», 1968)
Tipo C: circolazione interumana, raramente causa infezioni che inoltre si rivelano essere di modesta gravità
▪ Non presentano sostanziali differenze antigeniche in H e NPandemie influenzali del XX secolo
La più famosa e grave pandemia influenzale fu
causata dalla influenza “spagnola”.
Nel 1918-1919 causò la morte di circa 40 milioni di
persone, assai più che la Prima Guerra Mondiale.Orthomyxovirus Patogenesi & immunità ▪ Contagio per via inalatoria (aerosols) o per contatto (mani) ▪ Breve incubazione (1-2 giorni) ▪ Iniziale infezione citocida del tratto respiratorio superiore (cellule ciliate, cellule secernenti muco) ▪ Possibile diffusione al tratto respiratorio inferiore (polmoni) dove rimane circoscritta ▪ La ridotta clearance batterica da parte dell’epitelio ciliato, unita alla aumentata adesività batterica, può causare superinfezioni batteriche (bronchite, polmonite) e mortalità in soggetti anziani, defedati o con affezioni respiratorie croniche ▪ Sintomatologia e durata (risoluzione spontanea in 5-7 giorni) della malattia dipendenti da azione Interferon (influenza virus è eccellente induttore di IF), dalla risposta cellulo-mediata (virus compromette macrofagi e linfociti T) e dall’entità del danno tessutale ▪ Risposta anticorpale specifica (in particolar modo, IgA anti-H e -N) per ciascun ceppo influenzale e protettiva (le re-infezioni sono rare)
Orthomyxovirus
Sindromi cliniche
▪ Breve periodo di incubazione (1-3 giorni)
▪ Prodromo (alcune ore): malessere, cefalea
▪ Influenza acuta negli adulti
▪ repentini attacchi febbrili, malessere, mialgia, gola
infiammata, tosse non produttiva, inappetenza
▪ febbre persiste per 3-6 giorni e, in assenza di complicazioni, si ha guarigione in 7-10 giorni
▪ Influenza acuta nei bambini (< 3aa)
▪ malattia acuta simile a quella degli adulti ma con febbre più alta (convulsioni), sintomi
gastrointestinali (dolori addominali, vomito), otite media, miosite e più frequentemente
croup
▪ Complicazioni (soprattutto negli anziani, defedati o con infezioni respiratorie croniche)
▪ polmonite virale primaria o batterica secondaria (S. pneumoniae, S. aureus, H. influenzae)
con espettorato produttivo e purulento
▪ miosite
▪ coinvolgimento cardiaco
▪ sindromi neurologiche (sindr. di Guillain–Barrè, encefalopatia, encefalite, sindrome di Reye)Orthomyxovirus
Epidemiologia
▪ Geografia
▪ ubiquitari
▪ maggiore prevalenza in Cina: elevata densità di popolazione, prossimità dell’uomo con
animali (maiali, volatili, anatre)
▪ malattia “stagionale”: maggiormente diffusa in inverno (maggiore frequentazione di
ambienti ad elevata densità di popolazione; ridotte difese immunitarie)
▪ Trasmissione
▪ mediante inalazione di aerosol (prodotto durante fonazione, tosse e respirazione)
▪ tramite fomites (mani)
▪ il virus predilige i climi freschi e poco umidi
▪ largamente diffuso nei bambini in età scolare
▪ Soggetti a rischio
▪ bambini: infezioni delle vie respiratorie (da asintomatiche a gravi)
▪ adulti
▪ ad alto rischio: anziani (elevata mortalità se età > 65 aa), immunocompromessi, pazienti
cardiopatici e respiratori cronici (compresi asmatici e fumatori), donne in gestazioneOrthomyxovirus
Diagnosi di laboratorio
▪ Diagnosi clinica in corso di epidemia
▪ Diagnosi di laboratorio: i) epidemiologica (tipizzazione
virus); ii) differenziale (vs. altri virus respiratori)
▪ Campioni clinici: secrezioni faringo-bronchiali
▪ Isolamento virale:
▪ in embrione di pollo (cavità amniotica)
▪ in colture primarie di rene di scimmia o cane (linea
Madin-Darby); CPE dopo 2 giorni
▪ necessaria per definire gli stipiti che dovranno
essere inseriti nel vaccino; le caratteristiche
antigeniche dei ceppi virali influenzali circolati
nell’ultima stagione influenzale rappresentano la
base per selezionare i ceppi da includere nel vaccino
dell’anno successivo
▪ Identificazione: ricerca di Ag in colture cellulari,
mediante immunofluorescenza, immunoenzimatica od
inibizione dell’emoagglutinazione
▪ Indagine sierologica (aumentato titolo Ab da fase acuta a
convalescenza) utile solo a fini epidemiologiciOrthomyxovirus
Controllo dell’infezione
TERAPIA
▪ Amantadina, rimantadina
▪ interagiscono con la proteina M2, inibendo così la
scapsidazione virale (solo vs. tipo A)
▪ Zanamivir (Relenza®), oseltamivir (Tamiflu®)
▪ analoghi dell’acido sialico, inibiscono N (tipi A e B);
H lega acido sialico con formazione di aggregati virali,
impedendo il rilascio cellulare dei virus neoformati
CONTROLLO
▪ E’ impossibile limitare la diffusione aerea del virus influenzale (igiene respiratoria, lavaggio delle mani)
▪ Il controllo ottimale è rappresentato dall’immunizzazione:
▪ naturale: in seguito ad un’esposizione primaria, è protettiva per lunghi periodi
▪ acquisita (raccomandabile per i soggetti a rischio):
▪ vaccino inattivato, composto da virus inattivati con un detergente (vaccino split, trivalente o
tetravalente) oppure dalle proteine H e N purificate (vaccino a sub-unità)
▪ vaccino virosomale, costituito da liposomi che nel loro doppio strato fosfolipidico incorporano
le proteine virali per ottenere una più elevata immunogenicità
▪ vaccino con virus vivi e attenuati (LAIV), preparato per riassortimento genico tra stipiti tipo A e
B «di laboratorio» (attenuati ed incapaci di replicare a 37°C) e stipiti «selvaggi» indicati da
OMS; somministrato come spray intranasale, in soggetti di età inferiore ai 60 anniPuoi anche leggere